Шляхи пентозних фаз та споріднених захворювань
The Шлях пентоз Фосфат, також відомий як відхилення монофосфату гексоз, є основним метаболічним шляхом, який має рибосоми як кінцевий продукт, необхідний для шляхів синтезу нуклеотидів і нуклеїнових кислот, таких як ДНК, РНК, АТФ, NADH, FAD і кофермент А.
Вона також продукує NADPH (нікотинамід аденин динуклеотид фосфат), що використовується в різних ферментативних реакціях. Цей маршрут дуже динамічний і здатний адаптувати свою продукцію в залежності від моментних потреб осередків.
АТФ (аденозинтрифосфат) вважається "енергетичною валютою" клітини, оскільки її гідроліз може бути пов'язаний з широким спектром біохімічних реакцій.
Таким же чином NADPH є другою важливою енергетичною валютою для відновного синтезу жирних кислот, синтезу холестерину, синтезу нейромедіаторів, фотосинтезу та детоксикації..
Хоча NADPH і NADH подібні за структурою, вони не можуть використовуватися як взаємозамінні в біохімічних реакціях. NADPH бере участь у використанні вільної енергії в окисленні певних метаболітів для відновного біосинтезу.
На відміну від цього, NADH бере участь у використанні вільної енергії від окислення метаболітів для синтезу АТФ.
Індекс
- 1 Історія та місце розташування
- 2 Функції
- 3 етапи
- 3.1 Окислювальна фаза
- 3.2 Неокислювальна фаза
- 4 Супутні захворювання
- 5 Посилання
Історія та місце розташування
Вказівки на існування цього маршруту почалися в 1930 році завдяки досліднику Отто Варбургу, якому йому приписують відкриття НАДП.+.
Певні спостереження дозволили виявити маршрут, зокрема продовження дихання в присутності інгібіторів гліколізу, таких як фторид-іон \ t.
Потім у 1950 році вчені Френк Діккенс, Бернард Хорекер, Фріц Ліпман і Ефраїм Ракер описали шлях пентозофосфату.
Тканини, що беруть участь у синтезі холестерину і жирних кислот, таких як молочні залози, жирова тканина і нирки, мають високі концентрації пентозофосфатних ферментів.
Печінка також є важливою тканиною для цього шляху: приблизно 30% окислення глюкози в цій тканині відбувається завдяки ферментам пентозофосфатного шляху.
Функції
Шлях пентозофосфату відповідає за підтримання гомеостазу вуглецю в клітці. Крім того, шлях синтезує попередники нуклеотидів і молекул, що беруть участь у синтезі амінокислот (структурних блоків пептидів і білків)..
Він є основним джерелом зниження потужності для ферментативних реакцій. Крім того, він забезпечує необхідні молекули для анаболічних реакцій і для захисних процесів від окисного стресу. Остання фаза траси є критичною в окисно-відновних процесах у стресових ситуаціях.
Фази
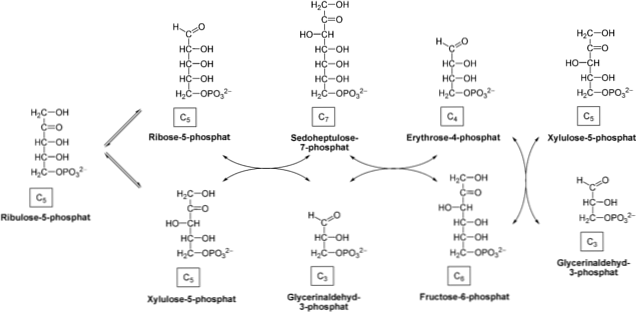
Шлях пентозофосфату складається з двох фаз в клітинному цитозолі: окислювальний, який генерує NADPH з окисленням глюкозо-6-фосфату до рибозо-5-фосфату; і неокислювальний, який передбачає взаємоперетворення цукрів трьох, чотирьох, п'яти, шести і семи вуглецевих.
Цей маршрут представляє спільні реакції з циклом Кальвіна і з шляху Ентнер-Дудороф, який є альтернативою гліколізу.
Окислювальна фаза
Окислювальна фаза починається з дегідрування молекули глюкозо-6-фосфату на вуглеці 1. Ця реакція каталізується ферментом глюкозо-6-фосфатдегідрогеназа, що має високу специфічність за NADP+.
Продуктом цієї реакції є 6-фосфоноглюконо-δ-лактон. Потім цей продукт гідролізується ферментом лактоназой, даючи 6-фосфоглюконат. Останнє з'єднання бере фермент 6-фосфоглюконат дегідрогеназу і перетворюється в рилулозу 5-фосфат.
Фермент фосфопентазоизомераза каталізує кінцевий етап окислювальної фази, яка передбачає синтез рибозо 5-фосфату шляхом ізомеризації рибулози 5-фосфату.
Ця серія реакцій продукує дві молекули NADPH і одну молекулу рибози 5-фосфату на молекулу глюкози 6-фосфату, що входить у цей ферментативний шлях.
У деяких клітинах вимоги NADPH більші, ніж вимоги рибози 5-фосфату. Отже, транскетолазние і трансальдолазние ферменти беруть рибозу 5-фосфат і перетворюють його в глицеральдегид 3-фосфат і фруктозу 6-фосфат, поступаючись місцем неокисляющей фазі. Ці останні два з'єднання можуть входити в гликолитический шлях.

Неокислювальна фаза
Фаза починається з реакції епімеризації, каталізованої ферментом пентезо-5-фосфат епімерази. Рибулозо-5-фосфат береться цим ферментом і перетворюється в ксилулозо-5-фосфат.
Продукт поглинається ферментом транскетолази, який діє спільно з коферментом тіаміну пірофосфатом (ТТР), який каталізує проходження ксилулозо-5-фосфату до рибозо-5-фосфату. З перенесенням кетози в альдозу виробляють гліцеральдегід-3-фосфат і седогептулоз-7-фосфат.
Далі, фермент трансальдолази переносить С3 з молекули седогептулоз-7-фосфату в гліцеральдегід-3-фосфат, який виробляє цукор з чотирьох вуглецю (еритро-4-фосфат) і цукор з 6 вуглецю (фруктоза-6). -фосфат). Ці продукти здатні підживлювати гліколітичний шлях.
Фермент transketosala діє знову для перенесення C2 ксилулозо-5-фосфату в еритро-4-фосфат, в результаті чого утворюється фруктоза-6-фосфат і глицеральдегид-3-фосфат. Як і на попередньому етапі, ці продукти можуть входити в гліколіз.
Ця друга фаза з'єднує шляхи, що генерують NADPH, з тими, хто відповідає за синтез АТФ і NADH. Крім того, продукти фруктозо-6-фосфату і глицеральдегид-3-фосфату можуть вводити глюконеогенез.
Супутні захворювання
Різні патології відносяться до шляху пентозофосфату, між цими нервово-м'язовими захворюваннями та різними типами раку.
Більшість клінічних досліджень орієнтовані на кількісну оцінку активності глюкозо-6-фосфатдегідрогенази, оскільки вона є головним ферментом, що відповідає за регулювання шляху.
У клітинах крові, що належать особам, чутливим до анемії, вони мають низьку ферментативну активність глюкозо-6-фосфатдегідрогенази. Навпаки, клітинні лінії, пов'язані з карциномами гортані, демонструють високу активність ферменту.
NADPH бере участь у виробництві глутатіону, ключової пептидної молекули в захисті від активних форм кисню, залучених до окисного стресу.
Різні типи раку призводять до активації пентозного шляху і пов'язані з метастазами, ангіогенезом і відповідями на хіміотерапію і радіотерапію.
З іншого боку, хронічне гранулематозне захворювання розвивається, коли є дефіцит у виробництві NADPH.
Список літератури
- Berg, J.M., Tymoczko, J.L., Stryer, L (2002). Біохімія. WH Freeman
- Konagaya, M., Konagaya, Y., Horikawa, H., & Iida, M. (1990). Пентазофосфатний шлях при нервово-м'язових захворюваннях - оцінка активності м'язової глюкози-6-фосфатдегідрогенази та вмісту РНК. Rinsho shinkeigak. Клінічна неврологія, 30(10), 1078-1083.
- Kowalik, M.A., Columbano, A., & Perra, A. (2017). Виникає роль пентозофосфатного шляху в гепатоцелюлярній карциномі. Кордони в онкології, 7, 87.
- Patra, К. C., & Hay, N. (2014). Пентазофосфатний шлях і рак. Тенденції в біохімічних науках, 39(8), 347-354.
- Stincone, A., Prigione, A., Cramer, T., Wamelink, M., Campbell, K., Cheung, E., ... & Keller, M.A. (2015). Повернення метаболізму: біохімія і фізіологія пентозофосфатного шляху. Біологічні огляди, 90(3), 927-963.
- Voet, D., & Voet, J.G. (2013). Біохімія. Видавець Artmed.


