Етилацетатна структура, властивості, синтез, застосування і ризики
The етилацетат або етиланоат (Назва IUPAC) - органічна сполука, хімічна формула якої є CH3COOC2H5. Він складається з ефіру, де спиртовий компонент походить від етанолу, а його компонент карбонової кислоти надходить з оцтової кислоти.
Це рідина при нормальних умовах температури і тиску, що надає фруктам приємний аромат. Ця властивість ідеально вступає в гармонію з тим, що очікується від складного ефіру; яка є фактично хімічною природою етилацетату. З цієї причини він знаходить застосування в харчових продуктах і алкогольних напоях.
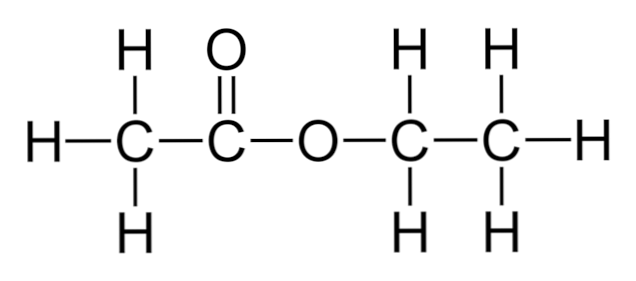
На верхньому зображенні показаний каркас структури етилацетату. Зверніть увагу на лівий компонент карбонової кислоти, а праворуч спиртову складову. З структурної точки зору можна очікувати, що ця сполука веде себе як гібрид між оцтом і спиртом; однак він має власні властивості.
Саме там такі гібриди, які називаються ефірами, виділяються як різні. Етилацетат не може реагувати як кислота і не може зневоднюватися у відсутності групи OH. Замість цього він проходить основний гідроліз в присутності сильного підстави, такого як гідроксид натрію, NaOH.
Ця реакція гідролізу використовується в навчальних лабораторіях для хімічних кінетичних експериментів; де реакція, крім того, є другого порядку. При гідролізі практично етиланоат повертається до вихідних компонентів: кислоти (депротонированний NaOH) і спирту.
У його структурному скелеті спостерігається, що атоми водню переважають над атомами кисню. Це впливає на їхню здатність взаємодіяти з неполярними видами, такими як жири. Він також використовується для розчинення сполук, таких як смоли, барвники, і в цілому органічні тверді речовини.
Незважаючи на приємний аромат, тривале вплив цієї рідини призводить до негативного впливу (як майже всіх хімічних сполук) в організмі..
Індекс
- 1 Структура етилацетату
- 1.1 Відсутність атомів донора водню
- 2 Фізико-хімічні властивості
- 2.1 Імена
- 2.2 Молекулярна формула
- 2.3 Молекулярна маса
- 2.4 Фізичне опис
- 2,5 Колір
- 2.6 Запах
- 2.7 Смак
- 2.8 Поріг запаху
- 2.9 Точка кипіння
- 2.10 Точка плавлення
- 2.11 Розчинність у воді
- 2.12 Розчинність в органічних розчинниках
- 2.13 Щільність
- 2.14 Щільність пари
- 2.15 Стабільність
- 2.16 Тиск пари
- 2.17 В'язкість
- 2.18 Теплота згоряння
- 2.19 Випаровування тепла
- 2.20 Поверхневий натяг
- 2.21 Індекс заломлення
- 2.22 Температура зберігання
- 2,23 pKa
- 3 Підсумок
- 3.1 Реакція Фішера
- 3.2 Реакція Тищенко
- 3.3 Інші методи
- 4 Використання
- 4.1 Розчинник
- 4.2 Штучні ароматизатори
- 4.3 Аналітика
- 4.4 Органічний синтез
- 4.5 Хроматографія
- 4.6 Ентомологія
- 5 Ризики
- 6 Посилання
Структура етилацетату
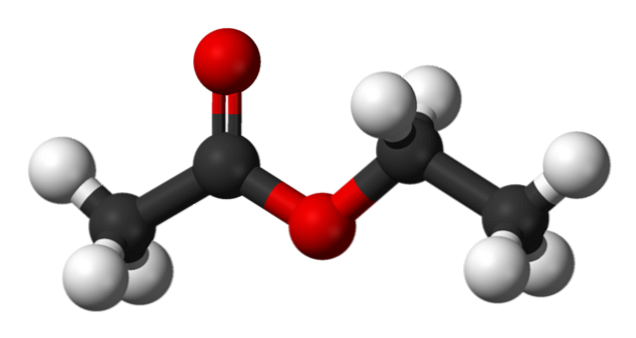
У верхньому зображенні структура етилацетату показана з моделлю сфер і грат. У цій моделі виділяються атоми кисню з червоними сферами; ліворуч - фракція, отримана з кислоти, а праворуч - фракція, отримана з спирту (алкокси-група, -OR).
Карбонільну групу оцінює зв'язок C = O (подвійні смуги). Структура навколо цієї групи і сусідній кисень є плоскою, оскільки відбувається делокалізація навантаження шляхом резонансу між обомами киснем; Факт, що пояснює відносно низьку кислотність α-водню (ті -CH групи3, пов'язані з C = O).
Молекула, обертаючи дві свої зв'язки, безпосередньо сприяє тому, як вона взаємодіє з іншими молекулами. Наявність двох атомів кисню, а також асиметрія в структурі, надають їй постійний дипольний момент; що, у свою чергу, відповідає за його диполь-дипольні взаємодії.
Наприклад, електронна щільність більша поблизу двох атомів кисню, значно зменшується в групі -CH3, і поступово в групі OCH2CH3.
Внаслідок цих взаємодій молекули етилацетату у звичайних умовах утворюють рідину, яка має високу температуру кипіння (77ºC)..
Відсутність донорних атомів водневих зв'язків
Якщо ви уважно подивитеся на структуру, ви помітите відсутність атома, здатного дарувати водневий міст. Проте атоми кисню є такими акцепторами, а етилацетат є дуже розчинним у воді і помітно взаємодіє з полярними сполуками і донорами водневих зв'язків (наприклад, цукрів)..
Також це дозволяє чудово взаємодіяти з етанолом; саме тому його присутність в алкогольних напоях не дивує.
З іншого боку, його алкоксигруппа робить його здатним взаємодіяти з деякими аполярними сполуками, такими як хлороформ, СН3Cl.
Фізико-хімічні властивості
Імена
-Етилацетат
-Етиланоат
-Ефір оцтової кислоти
-Ацетоксиэтан
Молекулярна формула
C4H8O2 або СН3COOC2H5
Молекулярна маса
88,106 г / моль.
Фізичний опис
Прозора безбарвна рідина.
Колір
Безбарвна рідина.
Запах
Характерні ефіри, схожі на запах ананаса.
Смак
Приємний при розведенні додає до пива фруктовий смак.
Поріг запаху
3,9 м.д. 0,0196 мг / м3 (низький запах); 665 мг / м3 (високий запах).
Виявлений запах при 7 - 50 ppm (середнє значення = 8 ppm).
Точка кипіння
Від 171 ° F до 760 мм Hg (77,1 ° C).
Точка плавлення
-118,5 ºF (-83,8 ºC).
Розчинність у воді
80 г / л.
Розчинність в органічних розчинниках
Змішується з етанолом і етиловим ефіром. Дуже розчинний в ацетоні і бензолі. Змішується також з хлороформом, фіксованими і леткими маслами, а також з окисленими і хлорованими розчинниками.
Щільність
0,9003 г / см3.
Щільність пари
3.04 (у співвідношенні повітря: 1).
Стабільність
Повільно розкладається з вологою; несумісні з декількома пластмасами і сильними окислювачами. Суміш з водою може бути вибухонебезпечною.
Тиск пари
93,2 мм рт.ст. при 25 ºC
В'язкість
0,423 мПуаз при 25 ºC.
Теплота згоряння
2,238,1 кДж / моль.
Випаровування тепла
35,60 кДж / моль при 25 ° С.
Поверхневий натяг
24 дин / см при 20 ºC.
Індекс заломлення
1,373 при 20 ºC / D.
Температура зберігання
2 - 8 ºC.
pKa
16 - 18 при 25 ° С.
Синтез
Реакція Фішера
Етилацетат синтезують промисловим шляхом за допомогою реакції Фішера, в якій етанол етерифікується оцтовою кислотою. Реакцію проводять при кімнатній температурі.
CH3CH2OH + CH3COOH <=> CH3COOCH2CH3 + H2O
Реакцію прискорюють за допомогою кислотного каталізу. Рівновага рухається вправо, тобто до виробництва етилацетату, шляхом видалення води; відповідно до Закону про масову акцію.
Реакція Тищенка
Етилацетат також готують промислово з використанням реакції Тищенко, кон'югуючи два еквівалента ацетальдегіду з використанням алкоксида в якості каталізатора.
2 CH3CHO => CH3COOCH2CH3
Інші методи
-Етилацетат синтезують як копродукт при окисленні бутану до оцтової кислоти, в реакції проводять при температурі 175 ° С і тиску 50 атм. В якості каталізатора використовуються іони кобальту та хрому.
-Етилацетат є співпродуктом етанолізу полівінілацетату з полівініловим спиртом.
-Етилацетат також продукується в промисловості шляхом дегідрування етанолу, причому реакція каталізується використанням міді при підвищеній температурі, але нижче 250 ° С..
Використання
Розчинник
Етилацетат використовують як розчинник і розчинник, використовуваний при очищенні друкованих плат. Використовується як розчинник у виробництві модифікованого екстракту хмелю, а також у декофеинизированном кавовому та чайному листках. Використовується в чорнилах, які використовуються для позначення фруктів і овочів.
Етилацетат використовується в текстильній промисловості в якості миючого засобу. Застосовується при калібруванні термометрів, що використовуються при поділі цукрів. У лакофарбовій промисловості він використовується як розчинник і розчинник використовуваних матеріалів.
Штучні ароматизатори
Використовується при розробці фруктових смаків; Наприклад: банан, груша, персик і ананас, а також аромат винограду і т.д..
Analytics
Застосовується при визначенні вісмуту, бору, золота, молібдену і платини, а також розчинника талію. Етилацетат має здатність витягувати багато сполук і елементів, присутніх у водному розчині, таких як: фосфор, кобальт, вольфрам і миш'як.
Органічні синтези
Етилацетат використовується в промисловості в якості редуктора в'язкості для смол, що використовуються в рецептурах фоторезисту. Його використовують у виробництві ацетаміду, ацетилацетату та метилгептанону.
Хроматографія
У лабораторіях етилацетат використовують в якості рухомої фази хроматографії на колонці і в якості екстракційного розчинника. Завдяки тому, що етилацетат має відносно низьку температуру кипіння, легко випаровується, що дозволяє концентрувати розчинені речовини в розчиннику.
Ентомологія
Етилацетат використовується в ентомології для задушення комах, поміщених в контейнер, що дозволяє проводити його збір і дослідження. Пари етилацетату вбивають комах, не руйнуючи його і запобігаючи його зміцненню, полегшуючи його збирання для збору.
Ризики
-LD50 етилацетату у щурів вказує на низьку токсичність. Однак він може дратувати шкіру, очі, шкіру, ніс і горло.
-Вплив високих рівнів може викликати запаморочення і непритомність. Крім того, тривале вплив може впливати на печінку і нирки.
-Вдихання етилацетату в концентрації 20 000 - 43 000 м.д. може викликати набряк легенів і крововилив.
-Ліміт професійної експозиції був встановлений OSHA при 400 ppm в повітрі, в середньому, протягом 8-годинної робочої зміни.
Список літератури
- Стівен А. Хардінгер. (2017). Ілюстрований глосарій органічної хімії: етилацетат (EtOAc). Отримано з: chem.ucla.edu
- Грем Соломонс Т.В., Крейг Б. Фріле. (2011). Органічна хімія. Аміни (10й видання.). Wiley Plus.
- Morrison, R.T. and Boyd, R.N. (1990). Органічна хімія (5та видання). Редакція Аддісон-Веслі Ібероамерикана.
- Вікіпедія. (2019). Етилацетат. Отримано з: en.wikipedia.org
- Cotton S. (s.f.). Етилацетат. Отримано з: chm.bris.ac.uk
- PubChem. (2019). Етилацетат. Отримано з: pubchem.ncbi.nlm.nih.gov
- Newseed Chemical. (2018). Застосування і застосування етилацетату. Отримано з: foodsweeteners.com
- Департамент охорони здоров'я старших служб Нью-Джерсі. (2002). Етилацетат. [PDF] Отримано з: nj.gov


