Історія калорій, частини, типи та їх характеристики
The калориметр є пристроєм, який використовується для вимірювання зміни температури певної кількості речовини (зазвичай води) відомої теплоємності. Ця зміна температури відбувається за рахунок поглинання або вивільнення тепла в досліджуваному процесі; хімічна, якщо вона є реакцією, або фізична, якщо вона складається з фази або зміни стану.
У лабораторії найпростіший калориметр, який можна знайти, - це чашка кави. Його використовують для вимірювання поглиненого або виділеного в реакції тепла при постійному тиску, у водному розчині. Реакції вибираються для уникнення втручання реагентів або газоподібних продуктів.
 У екзотермічній реакції кількість виділеного тепла можна розрахувати з підвищення температури калориметра і водного розчину:
У екзотермічній реакції кількість виділеного тепла можна розрахувати з підвищення температури калориметра і водного розчину:
Кількість тепла, що виділяється в реакції = кількість тепла, що поглинається калориметром + кількість тепла, що поглинається розчином
Кількість тепла, що поглинається калориметром, називається калорійністю калориметра. Це визначається подачею відомої кількості тепла в калориметр з заданою масою води. Потім вимірюють підвищення температури калориметра і розчину, який він містить.
За допомогою цих даних і використання питомої теплоти води (4,18 Дж / гС) можна розрахувати калорійність калориметра. Ця ємність також називається постійною калориметром.
З іншого боку, тепло, отримане водним розчином, дорівнює m · ce · Δt. У формулі m = маса води, ce = питома теплота води і Δt = зміна температури. Знаючи все це, можна розрахувати кількість тепла, що виділяється при екзотермічній реакції.
Індекс
- 1 Історія калориметра
- 2 частини
- 3 Типи та їх характеристики
- 3.1 Чашка кави
- 3.2 Калориметричний насос
- 3.3 Адиабатичний калориметр
- 3.4 Ізоперіболічний калориметр
- 3.5 Поточний калориметр
- 3.6 Калориметр для диференціальної скануючої калориметрії
- 4 Програми
- 4.1 У фізико-хімії
- 4.2 У біологічних системах
- 4.3 Калориметр кисневого насоса і калорійність
- 5 Посилання
Історія калориметра
У 1780 році французький хімік А. Л. Лавуазьє, який вважався одним з батьків хімії, використовував морську свинку для вимірювання виробництва тепла своїм диханням..
Як? Використання пристрою, подібного калориметру. Тепло, яке вироблялося морським свинкам, було підтверджено таненням снігу, який оточував апарат.
Дослідники А. Л. Лавуазьє (1743-1794) і П. С. Лаплас (1749-1827) розробили калориметр, який використовувався для вимірювання питомої теплоти тіла методом плавлення льоду.
Калориметр складався з олов'яного циліндричного стакана, лакованого, триманого штативом і внутрішньо завершеного воронкою. Всередині було поміщено ще одне скло, подібне до попереднього, з трубкою, що пройшла через зовнішню камеру, і була забезпечена ключем. Усередині друге скло було сіткою.
У цю сітку розміщувалося буття або об'єкт, чию питому теплоту бажано було визначити. Лід поміщали всередину концентричних судин, як у кошику.
Тепло, яке виробляється тілом, поглинається льодом, викликаючи його злиття. І рідкий водний продукт плавлення льоду збирали, відкриваючи ключ внутрішнього скла.
І, нарешті, зважуючи воду, масу розплавленого льоду було відомо.
Частини
Найбільш часто використовуваним калориметром в навчальних лабораторіях хімії є так званий калориметр чашки кави. Цей калориметр складається з мензурки, або замість нього, контейнера з анімовим матеріалом, який має певні ізолюючі властивості. Всередині цього контейнера водний розчин поміщається в тіло, яке виробляє або поглинає тепло.
У верхній частині контейнера розміщена кришка ізоляційного матеріалу з двома отворами. В одному термометрі вводять для вимірювання зміни температури, а в іншому мішалку, переважно зі скляного матеріалу, який виконує функцію переміщення вмісту водного розчину..
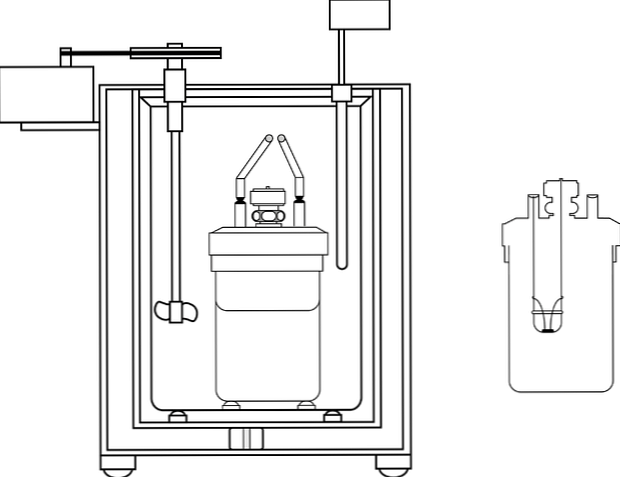
На зображенні показані частини калориметричного насоса; однак, можна помітити, що він має термометр і мішалку, загальні елементи в кількох калориметрах.
Типи та їх характеристики
Чашка кави
Це той, який використовується для визначення тепла, що виділяється при екзотермічній реакції, і тепла, що поглинається в ендотермічній реакції.
Крім того, він може бути використаний при визначенні питомої теплоти тіла; тобто кількість тепла, яку грам речовини повинен поглинати, щоб підняти його температуру на один градус Цельсія. .
Калориметричний насос
Це пристрій, в якому вимірюється кількість тепла, що виділяється або поглинається в реакції, що відбувається при постійному об'ємі.
Реакція протікає в міцному сталевому посудині (насос), який занурюється у великий об'єм води. Це робить зміни температури води невеликими. Тому передбачається, що зміни, пов'язані з реакцією, вимірюються при постійній температурі і об'ємі.
Вищевказане вказує на те, що жодна робота не виконується, коли реакцію проводять в калориметричному насосі.
Реакція починається шляхом подачі електроенергії через кабелі, підключені до насоса.
Адиабатичний калориметр
Вона характеризується наявністю ізолюючої структури, що називається щитом. Щит розташований навколо клітини, де відбуваються зміни тепла і температури. Він також з'єднаний з електронною системою, яка підтримує свою температуру дуже близько до температури електролізера, щоб уникнути передачі тепла.
У адіабатичному калориметрі різниця температур між калориметром і його оточенням зводиться до мінімуму; а також мінімізація коефіцієнта теплопередачі та часу на теплообмін.
Його частини складаються з наступного:
-Осередок (або контейнер), інтегрований в систему ізоляції, за допомогою якої він намагається уникнути втрат тепла.
-Термометр, для вимірювання зміни температури.
-Нагрівач, підключений до керованого джерела електричної напруги.
-І щит, вже згадуваний.
У цьому типі калориметра можуть бути визначені такі властивості, як ентропія, температура Дебая та щільність електронного стану.
Ізоперіболічний калориметр
Це пристрій, в якому реакційна комірка і насос занурюються в структуру, яка називається сорочкою. У цьому випадку так звана сорочка складається з води, що зберігається при постійній температурі.
Температура електролізера і насоса зростають при виділенні тепла під час процесу горіння; але температура водяної сорочки підтримується при фіксованій температурі.
Мікропроцесор контролює температуру комірки і сорочки, роблячи необхідні корекції тепла витоку, що є наслідком відмінностей між двома температурами.
Ці виправлення застосовуються безперервно і з остаточної корекцією на основі вимірювань до і після випробування.
Потік калориметра
Розроблений Caliendar, він має пристрій для переміщення газу в контейнері з постійною швидкістю. При додаванні тепла вимірюється підвищення температури в рідині.
Потік калориметра характеризується:
- Точне вимірювання постійної швидкості потоку.
- Точне вимірювання кількості тепла, що вводиться в рідину через нагрівач.
- Точне вимірювання збільшення температури в газі, що викликається введеною енергією
- Конструкція для вимірювання ємності газу під тиском.
Калориметр для диференціальної скануючої калориметрії
Характеризується наявністю двох контейнерів: в одному місці досліджуваного зразка розміщується, а інший зберігається порожнім або використовується довідковий матеріал..
Два судини нагріваються з постійною енергією, за допомогою двох незалежних нагрівачів. Коли починається нагрів двох контейнерів, комп'ютер відображає різницю теплового потоку нагрівачів проти температури, таким чином, визначаючи потік тепла.
Крім того, можна визначити зміну температури як функцію часу; і, нарешті, калорійність.
Програми
У фізико-хімії
-Основні калориметри, тип чашки кави, дозволяють виміряти кількість тепла, що вивільняється або поглинається тілом. Вони можуть визначити, чи є реакція екзотермічною або ендотермічною. Крім того, можна визначити питому теплоту тіла.
-За допомогою адиабатичного калориметра можна було визначити ентропію хімічного процесу та електронну щільність стану.
У біологічних системах
-Мікрокалориметри використовуються для вивчення біологічних систем, які включають взаємодії між молекулами, а також молекулярні конформаційні зміни, які відбуваються; наприклад, при розгортанні молекули. Лінія включає як диференціальне сканування, так і ізотермічне титрування.
-Мікрокалориметр використовується при розробці лікарських засобів малих молекул, біотерапевтичних препаратів і вакцин.
Калориметр кисневого насоса та калорійність
Спалювання численних речовин відбувається в калориметрі кисневого насоса, і його калорійну потужність можна визначити. До числа речовин, що вивчаються за допомогою цього калориметра, належать: вугілля і кокс; харчові олії, як важкі, так і легкі; бензину і всіх моторних палив.
А також види палива для авіаційних реакторів; відходи палива та утилізація відходів; харчові продукти та добавки для харчування людини; кормові культури та добавки для кормів для тварин; будівельні матеріали; ракетно-пальне.
Аналогічно калорійну потужність визначали за допомогою калориметрії в термодинамічних дослідженнях горючих матеріалів; у вивченні енергетичного балансу в екології; у вибухових і теплових порошках і в навчанні основних термодинамічних методів.
Список літератури
- Уіттен, Девіс, Пек і Стенлі. Хімія (8-е изд.). CENGAGE Навчання.
- González J., Cortés L. & Sánchez A. (s.f.). Адиабатическая калориметрія та її застосування. Відновлено з: cenam.mx
- Вікіпедія. (2018). Калориметр. Отримано з: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (22 червня 2018). Визначення калориметра в хімії. Отримано з: thoughtco.com
- Гіллеспі, Клер. (11 квітня 2018). Як працює калориметр? Наука. Отримано з: sciencing.com


