Сильні і слабкі електроліти, відмінності, приклади
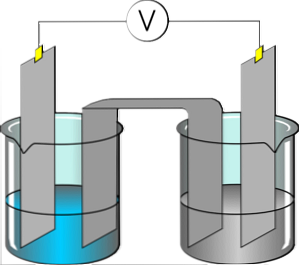
The електроліти вони являють собою речовини, які виробляють електропровідний розчин при розчиненні в полярному розчиннику, такому як вода. Розчинний електроліт розділяється на катіони і аніони, які дисперговані у зазначеному розчині. Якщо до розчину застосований електричний потенціал, катіони будуть прилипати до електрода, що має велику кількість електронів.
Навпаки, аніони в розчині зв'язуються з електродефіцитним електродом. Речовина, що дисоціює на іони, набуває здатність проводити електрику. Більшість солей, кислот і розчинних основ являють собою електроліти.
Деякі гази, такі як хлористий водень, можуть діяти як електроліти при певних умовах температури і тиску. Натрій, калій, хлорид, кальцій, магній і фосфат є гарним прикладом електролітів.
Індекс
- 1 Що таке сильні і слабкі електроліти?
- 2 Відмінності
- 3 Методи ідентифікації електролітів
- 4 Приклади сильних і слабких електролітів
- 4.1 Сильні електроліти
- 4.2 Слабкі електроліти
- 5 Посилання
Що таке сильні і слабкі електроліти?
The сильні електроліти це ті, які повністю іонізують - тобто вони 100% розділені - у той час як слабкі електроліти вони іонізуються лише частково. Цей відсоток іонізації зазвичай становить від 1 до 10%.
Для кращої диференціації цих двох типів електролітів можна сказати, що в розчині сильного електроліту основними видами (або видами) є отримані іони, а в розчині слабкого електроліту основним видом є саме з'єднання. іонізувати.
Сильні електроліти діляться на три категорії: сильні кислоти, сильні основи і солі; при цьому слабкі електроліти діляться на слабкі кислоти і слабкі основи.
Всі іонні сполуки є сильними електролітами, тому що вони розділяються на іони, коли вони розчиняються у воді.
Навіть найбільш нерозчинні іонні сполуки (AgCl, PbSO4, CaCO3) є сильними електролітами, тому що невеликі кількості, які розчиняються у воді, роблять це переважно у вигляді іонів; тобто відсутня дисоційована форма або кількість сполуки в отриманому розчині.
Еквівалентна провідність електролітів зменшується при більш високих температурах, але поводиться по-різному в залежності від їх міцності.
Сильні електроліти мають більш низьке зниження їх провідності при більш високих концентраціях, а слабкі електроліти мають велику швидкість зниження електропровідності при більш високих концентраціях..
Відмінності
Важливо знати, як розпізнати формулу і визнати, в якій її класифікації (іон або з'єднання), оскільки це буде залежати від стандартів безпеки при роботі з хімічними речовинами.
Як було сказано раніше, електроліти можуть бути визначені як сильні або слабкі в залежності від їх іонізаційної здатності, але це іноді може бути більш очевидним, ніж здається.
Більшість кислот, основ і розчинних солей, які не являють собою кислоти або слабкі основи, вважаються слабкими електролітами.
Фактично, слід припустити, що всі солі є сильними електролітами. Навпаки, слабкі кислоти і основи, крім азотовмісних сполук, вважаються слабкими електролітами.
Методи ідентифікації електролітів
Існують способи для полегшення ідентифікації електролітів. Далі використовується шестиступінчастий метод:
- Чи є ваш електроліт однією з семи сильних кислот?
- Це металева форма (OH)n? Тоді це сильна основа.
- Це металева форма (X)n? Тоді це сіль.
- Ваша формула починається з H? Тоді це, мабуть, слабка кислота.
- Чи має він атом азоту? Тоді вона може бути слабкою базою.
- Жодне з наведеного вище не застосовується? Тоді це не електроліт.
Також, якщо реакція, представлена електролітом, виглядає наступним чином: NaCl (s) → Na+(ac) + Cl-(ac), в якому реакція розмежована прямою реакцією (→), мова йде про сильному електроліті. У випадку, якщо вона обмежена непрямим (↔), то це слабкий електроліт.
Як зазначено в попередньому розділі, провідність електроліту змінюється в залежності від концентрації цього в розчині, але і це значення залежить від міцності електроліту..
При більш високих концентраціях сильні і проміжні електроліти не зменшуються в значних інтервалах, але слабкі будуть представляти високе зниження до досягнення значень, близьких до нуля, при більш високих концентраціях..
Є також проміжні електроліти, які можуть бути дисоційовані в розчинах при більш високих відсотках (менше 100%, але більше 10%), крім неелектролітів, які просто не дисоціюють (сполуки вуглецю, такі як цукру, жири і спирти)..

Приклади сильних і слабких електролітів
Сильні електроліти
Сильні кислоти:
- Перхлорна кислота (HClO4)
- Бромистоводородная кислота (HBr)
- Соляна кислота (HCl)
- Сірчана кислота (Н2SO4)
- Азотна кислота (HNO)3)
- Періодична кислота (HIO)4)
- Фтороантимоновая кислота (HSbF)6)
- Магічна кислота (SbF)5)
- Фтористая кислота (FSO)3H)
Міцні основи
- Гідроксид літію (LiOH)
- Гідроксид натрію (NaOH)
- Гідроксид калію (KOH)
- Гідроксид рубідію (RbOH)
- Гідроксид цезію (CsOH)
- Гідроксид кальцію (Ca (OH))2)
- Гідроксид стронцію (Sr (OH))2)
- Гідроксид барію (Ba (OH))2)
- Амід натрію (NaNH)2)
Сильні продажі
- Хлорид натрію (NaCl)
- Нітрат калію (KNO)3)
- Хлорид магнію (MgCl2)
- Ацетат натрію (СН3COONa)
Слабкі електроліти
Слабкі кислоти
- Оцтова кислота (СН3COOH)
- Бензойна кислота (С6H5COOH)
- Мурашина кислота (HCOOH)
- Ціанід водню (HCN)
- Хлороцтову кислоту (СН2ClOOH)
- Йодна кислота (HIO)3)
- Азотна кислота (HNO2)
- Вуглекислота (H2CO3)
- Фосфорна кислота (Н3PO4)
- Сірчана кислота (Н2SO3)
Слабкі основи та сполуки азоту
- Диметиламин ((СН3)2NH)
- Етиламін (C2H5NH2)
- Аміак (NH3)
- Гідроксиламін (NH2OH)
- Піридин (C5H5N)
- Анілін (C6H5NH2)
Список літератури
- Сильний електроліт. Отримано з en.wikipedia.org
- Anne Helmenstine, P. (s.f.). Наукові записки Отримано з sciencenotes.org
- OpenCourseWare. (s.f.). Умасс Бостон. Отримано з ocw.umb.edu
- Хімія, D. o. (s.f.). Коледж св. Олафа. Отримано з stolaf.edu
- Anne Marie Helmenstine, P. (s.f.). ThoughtCo. Отримано з thoughtco.com


