Хімічна структура, властивості та застосування фенантрена
The фенантрен це вуглеводень (у своєму складі він має вуглець і водень), фізичні та хімічні властивості яких вивчаються органічною хімією. Він належить до групи так званих ароматичних сполук, фундаментальною структурною одиницею яких є бензол.
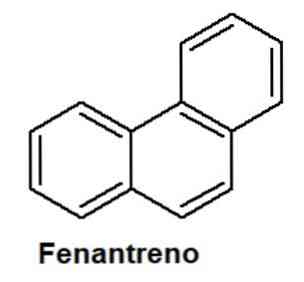
Ароматичні сполуки також включають злиті поліциклічні сполуки, утворені кількома ароматичними кільцями, які мають зв'язок вуглець-вуглець (С-С). Фенантрен є одним з них, у його структурі є три злиті кільця. Вона вважається ізомером антрацену, сполуки, що має три кільця, сплавлені лінійно.
Він був виділений з антраценового масла з кам'яновугільної смоли. Вона отримується шляхом перегонки деревини, викидів транспортних засобів, розливів нафти та інших джерел..
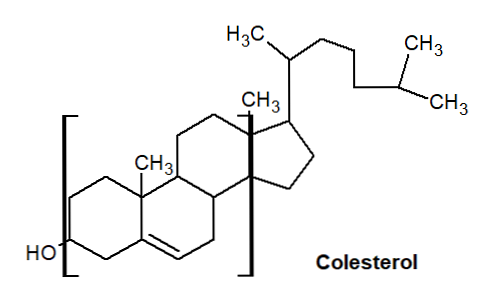
Він знаходиться в середовищі через сигаретний дим, і в стероїдних молекулах він утворює ароматичну основу хімічної структури, як показано на молекулі холестерину.
Індекс
- 1 Хімічна структура
- 2 Фізико-хімічні властивості
- 3 Використання
- 3.1 Фармакологія
- 4 Вплив на здоров'я
- 5 Посилання
Хімічна структура
Фенантрен має хімічну структуру, утворену трьома бензольними кільцями, сплавленими разом вуглець-вуглецевим зв'язком.
Вона вважається ароматичною структурою, тому що вона відповідає Закону Хюкле про ароматичність, який говорить: «Сполука є ароматичною, якщо вона має 4n + 2 pi (π) делокалізованих і спряжених (змінних) електронів, з сигма-електронами (σ) прості посилання.
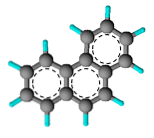
При застосуванні закону Хюкеля до структури фенантрену і з урахуванням того, що n відповідає кількості бензольних кілець у структурі, виявляється, що 4n + 2 = 4 (3) +2 = 16 електронів π. Вони розглядаються як подвійні зв'язки в молекулі.
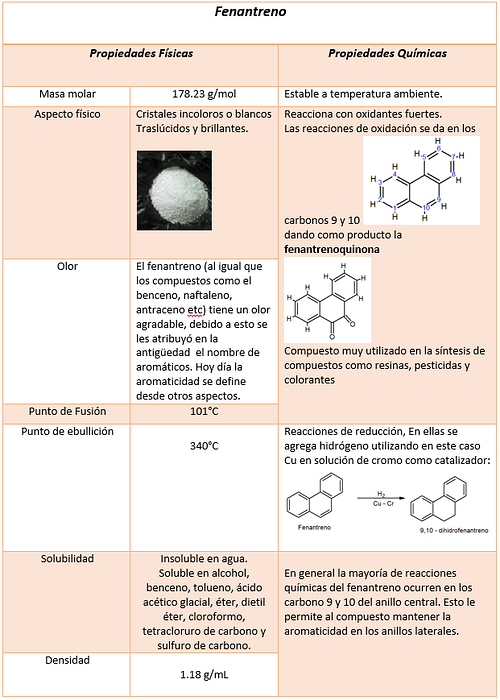
Фізико-хімічні властивості
-Щільність 1180 кг / м3; 1,18 г / см3
-Температура плавлення 489,15 К (216 ° С)
-Точка кипіння 613,15 К (340 ° С)
Властивості сполуки є характеристиками або якостями, які дозволяють його диференціювати від інших. Властивості, які вимірюються сполукою, є фізичними властивостями та хімічними властивостями.
Хоча фенантрен є ізомерною формою антрацену, його властивості дуже різні, що дає фенантрен більшу хімічну стабільність завдяки кутовому положенню одного з його ароматичних кілець..
Використання
Фармакологія
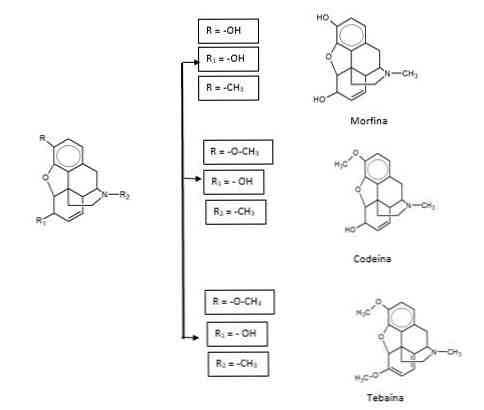
Опіоїдні препарати можуть бути природного походження або похідними фенантрена. Серед них морфін, кодеїн і тебаїн.
Найбільш репрезентативні використання фенантрену отримують, коли воно знаходиться в окисленій формі; тобто як фенантренхінон. У цьому способі його можна використовувати в якості барвників, лікарських засобів, смол, фунгіцидів і в інгібуванні полімеризації деяких процесів. 9,10-бифенилдикарбоновую кислоту використовують для отримання поліефірної та алкідної смоли.
Вплив на здоров'я
Не тільки фенантрен, але і всі поліциклічні ароматичні вуглеводні, як правило, відомі як ПАУ, є токсичними і шкідливими для здоров'я. Вони знаходяться у воді, на землі та в повітрі в результаті згорання, розливів нафти або як продукт реакцій в промисловому полі.
Токсичність зростає, оскільки їхні ланцюги з злитими бензольними кільцями стають більшими, хоча це не означає, що коротколанцюгові ПАУ не є..
З бензолу, який є фундаментальною структурною одиницею цих сполук, вже відома його висока токсичність і мутагенна активність у живих істотах.
Нафталін, що називається проти молі, використовується як контроль над шкідниками, які атакують тканини одягу. Антрацен - це мікробіцид, що використовується у вигляді таблеток для протидії запахам, викликаним бактеріями.
У випадку фенантрена він накопичується в жирових тканинах живих істот, виробляючи токсичність, коли людина піддається впливу забруднювача протягом тривалого часу.
На додаток до цих ефектів можна назвати такі:
- Це паливо.
- Після тривалих періодів впливу фенантрену індивідуум може кашляти, респіраторна задишка, бронхіт, подразнення дихальних шляхів і подразнення шкіри..
- При нагріванні до розкладання, може викликати подразнення шкіри і дихальних шляхів через випромінювання щільного і задушливого диму.
- Може реагувати з сильними окислювачами.
- У разі пожежі за допомогою цього з'єднання можна керувати сухим діоксидом вуглецю, галоном галону або водою.
- Його слід зберігати в прохолодному місці, в герметичних контейнерах і подалі від окислювальних речовин.
- Необхідно використовувати засоби індивідуального захисту (MMP), криту взуття, фартух з довгими рукавами та рукавички.
- Згідно з даними Національного інституту охорони праці та охорони праці, для поводження з компанією слід використовувати маску з напівфабрикатами, оснащену фільтрами проти туману та інший спеціальний фільтр для хімічних парів..
- У разі подразнення очей та / або шкіри рекомендується промити великою кількістю води, вилучити забруднену одяг або аксесуари, а у дуже важких випадках звернутися за медичною допомогою до пацієнта..
Список літератури
- ScienceDirect, (2018), фенантрен, відновлений, 26 травня 2018, sciencedirect.com
- Mastandrea, C., Chichizola, C., Ludueña, B., Sánchez, H., Alvarez, H., Gutiérrez, A., (2005). Поліциклічні ароматичні вуглеводні. Ризики для здоров'я та біологічні маркери, Закон Латинської Америки про клінічну біохімію, том 39,1, scielo.org.ar
- Beyer, H., Wolfgang, W., (1987), Посібник з органічної хімії, (E-Book), books.google.com.co
- Cheimicalbook, (s.f), фенантрен, фенантрен Хімічні властивості та інформація з техніки безпеки, відновлені, 26 березня 2018, chemicalbook.com
- Fernández, P L., (1996), Фармакологічне лікування болю, опіатні препарати, отримані з фенантрена, UCM, Мадрид, [PDF], ucm.es, revistas.ucm.es
- Cameo Chemicals, (s.f), фенантрен, інформаційний лист і безпека, вилучено, 27 березня 2018 р., cameochemicals.noaa.gov
- Моррісон Р., Бойд Р. (1998), Органічна хімія (5-е видання), Мексика, Міжамериканський освітній фонд, С.А.
- Pine, S., Hammond, G., Cram, D., Hendrickson, J., (1982). Química Orgánica, (друге видання), Мексика, McGraw-Hill de México, S.A de C.V
- Chemsketch. Програмне забезпечення, що використовується для написання формул і молекулярних структур різних хімічних сполук. Настільне додаток.


