Структура гідроксиду амонію, властивості, номенклатура, застосування
The гідроксид амонію являє собою з'єднання молекулярної формули NH4OH або H5НЕ виробляється розчиненням аміачного газу (NH3) у воді. З цієї причини він отримує назви аміачної води або рідкого аміаку.
Це безбарвна рідина з дуже інтенсивним і різким запахом, що не ізолює. Ці характеристики мають прямий зв'язок з концентрацією NH3 розчинений у воді; Концентрація, яка насправді, будучи газом, може охоплювати величезні її кількості, розчинені в невеликому обсязі води.
Значно менша частина цих водних розчинів складається з катіонів NH4+ і OH-аніони-. З іншого боку, в дуже розбавлених розчинах або в заморожених твердих речовинах при дуже низьких температурах аміак можна знайти у вигляді гідратів, таких як: NH3. H2O, 2NH3. H2O і NH3H 2H2O.
Як цікавий факт, хмари Юпітера утворюються розведеними розчинами гідроксиду амонію. Однак космічний зонд Галілео не зміг знайти воду в хмарах планети, що можна було очікувати від знання того, що утворення гідроксиду амонію відомо; тобто вони є кристалами NH4OH повністю безводний.
Іон амонію (NH4+) виробляється в просвіті трубчастої нирки шляхом об'єднання аміаку і водню, секретованого нирковими трубчастими клітинами. Аналогічно, амоній утворюється в ниркових трубчастих клітинах в процесі перетворення глутаміну в глутамат і, в свою чергу, у перетворенні глутамату в α-кетоглутарат.
Аміак виробляють промисловим способом за методом Хабера-Боша, в якому реагують гази азоту і водню; використовують іон тривалентного заліза, оксид алюмінію і оксид калію в якості каталізаторів. Реакцію проводять при високих тисках (150 - 300 атмосфер) і високих температурах (400-500 ºС), з виходом 10-20%..
У реакції утворюється аміак, який при окисленні продукує нітрити і нітрати. Це важливо для отримання азотної кислоти та добрив, таких як аміачна селітра.
Індекс
- 1 Хімічна структура
- 1.1 Амонячний лід
- 2 Фізико-хімічні властивості
- 2.1 Молекулярна формула
- 2.2 Молекулярна маса
- 2.3 Зовнішній вигляд
- 2.4 Концентрація
- 2.5 Запах
- 2.6 Смак
- 2.7 Порогове значення
- 2.8 Температура кипіння
- 2.9 Розчинність
- 2.10 Розчинність у воді
- 2.11 Щільність
- 2.12 Щільність пари
- 2.13 Тиск пари
- 2.14 Корозійна дія
- 2,15 рН
- 2.16 Константа дисоціації
- 3 Номенклатура
- 4 Розчинність
- 5 Ризики
- 5.1 Реактивність
- 6 Використання
- 6.1
- 6.2 Терапевтичні засоби
- 6.3 Промислове та інше
- 6.4 У сільському господарстві
- 7 Посилання
Хімічна структура
Як зазначено в його визначенні, гідроксид амонію складається з водного розчину газоподібного аміаку. Тому в рідині відсутня певна структура, яка відрізняється від структури випадкового розташування іонів NH4+ і OH- сольватированних молекулами води.
Амонійні та гідроксильні іони є продуктами рівноваги гідролізу аміаку, тому загальні для цих розчинів мають різкий запах:
NH3(g) + H2O (l) <=> NH4+(ac) + OH-(ac)
Згідно з хімічним рівнянням, високе зниження концентрації води змістило б рівновагу до утворення більшої кількості аміаку; тобто при нагріванні гідроксиду амонію випаровуються пари аміаку.
З цієї причини іони NH4+ і OH- вони не встигають утворювати кристал в земних умовах, що приводить як наслідок, що тверда основа NH4OH не існує.
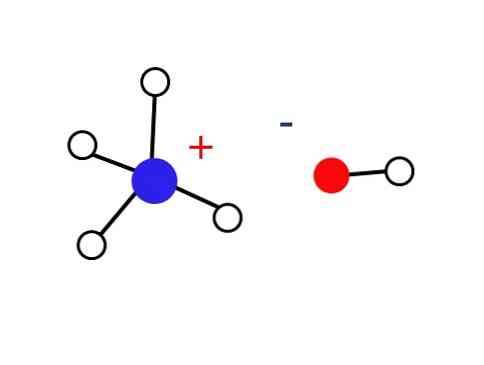
Це тверде тіло повинно складатися тільки з іонів, які взаємодіють електростатично (як показано на зображенні).
Амонячний лід
Тим не менш, при температурі нижче 0ºC, і в оточенні величезних тисків, таких як ті, що переважають в ядрах крижаних місяців, амоній і вода замерзають. При цьому вони кристалізуються в твердій суміші з різними стехіометричними пропорціями, що є найпростішим NH3. H2O: моногідрат аміаку.
NH3. H2O і NH3H 2H2Або вони є аміачним льодом, тому що тверда речовина складається з кристалічного розташування молекул води і аміаку, з'єднаного водневими зв'язками..
Враховуючи зміну T і P, згідно з обчислювальними дослідженнями, які імітують всі фізичні змінні та їх вплив на цей лід, відбувається перехід фази NH.3. NH2Або до фази NH4OH.
Тому тільки в цих екстремальних умовах NH4OH може існувати як продукт протонування в льоду між NH3 і Н2O:
NH3(s) + H2O (s) <=> NH4OH (s)
Зауважимо, що на цей раз, на відміну від гідролізу аміаку, задіяні види знаходяться в твердій фазі. Аміачний лід, що стає солоним, не випускаючи аміак.
Фізико-хімічні властивості
Молекулярна формула
NH4OH або H5NO
Молекулярна маса
35,046 г / моль
Зовнішній вигляд
Це безбарвна рідина.
Концентрація
До приблизно 30% (для іонів NH4+ і OH-).
Запах
Дуже сильний і гострий.
Смак
Акр.
Порогове значення
34 ppm для неспецифічного виявлення.
Точка кипіння
38 ºC (25%).
Розчинність
Він існує тільки у водному розчині.
Розчинність у воді
Змішується в необмежених пропорціях.
Щільність
0,90 г / см3 при 25 ºC.
Щільність пари
Щодо повітря, прийнятого за одиницю: 0,6. Тобто вона менш щільна, ніж повітря. Однак, логічно, що вказана величина відноситься до аміаку як газу, а не до його водних розчинів або до NH4OH.
Тиск пари
2,160 мм рт.ст. при 25 ºC.
Корозійна дія
Він здатний розчиняти цинк і мідь.
рН
11,6 (розчин 1 N); 11.1 (розчин 0.1 N) і 10,6 (0,01 Н розчин).
Константа дисоціації
pKb = 4,767; Kb = 1,71 x 10-5 при 20 ºC
pKb = 4,751; Kb = 1,774 x 10-5 при 25 ° С.
Підвищення температури майже непомітно підвищує основність гідроксиду амонію.
Номенклатура
Які загальні та офіційні назви отримує NH?4OH? Згідно з тим, що встановлено IUPAC, його назвою є гідроксид амонію, оскільки він містить гідроксильний аніон.
Амоній за своїм навантаженням +1 є моновалентним, тому при використанні номенклатури запасів він називається: гідроксид амонію (I).
Хоча використання терміну гідроксид амонію є технічно некоректним, оскільки з'єднання не ізолюється (щонайменше, не на Землі, як детально пояснено в першому розділі).
Крім того, гідроксид амонію отримує назви аміачної води і рідкого аміаку.
Розчинність
NH4ОН, оскільки солі немає в земних умовах, не можна оцінити, наскільки розчинний він в різних розчинниках.
Проте можна було б очікувати, що він буде надзвичайно розчинний у воді, оскільки його розчинення вивільнить величезні кількості NH3. Теоретично це було б дивовижним способом зберігання та транспортування аміаку.
В інших розчинниках, здатних приймати водневі зв'язки, такі як спирти і аміни, можна очікувати, що вони також будуть дуже розчинними в них. Тут NH катіон4+ є донором водневих мостів і OH- він працює як обидва.
Прикладами цих взаємодій з метанолом були б: Н3N+-H - OHCH3 і HO- - HOCH3 (OHCH3 вказує, що кисень отримує водневу зв'язок, а не те, що метильна група пов'язана з H).
Ризики
-При контакті з очима викликає роздратування, що може призвести до пошкодження очей.
-Він є корозійним. Тому при контакті з шкірою може викликати подразнення і при високих концентраціях реагенту, викликає опіки шкіри. Повторний контакт гідроксиду амонію з шкірою може викликати його сухість, свербіж і почервоніння (дерматит).
-Вдихання спрею гідроксиду амонію може викликати гостре подразнення дихальних шляхів, що характеризується задухами, кашлем або задишкою. Тривале або повторне опромінення речовини може призвести до повторних бронхіальних інфекцій. Також вдихання гідроксиду амонію може викликати подразнення легенів.
-Вплив високих концентрацій гідроксиду амонію може бути надзвичайним, оскільки накопичення рідини в легенях (набряк легенів) може виникнути.
-Концентрація 25 ppm була взята в якості межі впливу, у 8-годинній робочій зміні, в середовищі, де працівник піддається дії шкідливої дії гідроксиду амонію.
Реактивність
-Крім того, про потенційну шкоду для здоров'я від впливу гідроксиду амонію існують інші запобіжні заходи, які необхідно враховувати при роботі з речовиною.
-Гідроксид амонію може реагувати з багатьма металами, такими як: срібло, мідь, свинець і цинк. Він також реагує з солями цих металів для утворення вибухонебезпечних сполук і вивільнення газоподібного водню; що, у свою чергу, є вогненебезпечним і вибухонебезпечним.
-Він може бурхливо реагувати з сильними кислотами, наприклад: соляною кислотою, сірчаною кислотою і азотною кислотою. Аналогічним чином він реагує таким же чином з диметилсульфатом і галогенами.
-Реагує з сильними підставами, такими як гідроксид натрію і гідроксид калію, виробляючи газоподібний аміак. Це можна перевірити, якщо спостерігається рівновага в розчині, в якому додають іони OH- зміщує баланс до утворення NH3.
-Мідні та алюмінієві метали, як і інші оцинковані метали, не повинні використовуватися при обробці гідроксидом амонію через його корозійну дію на них..
Використання
У їжу
-Використовується як добавка в багатьох харчових продуктах, в яких вона діє як розпушувач, рН-контроль і фінішний агент харчової поверхні..
-Перелік продуктів, в яких використовується гідроксид амонію, є великим і включає хлібобулочні вироби, сири, цукерки, цукерки та пудинги.
-Гідроксид амонію класифікується FDA як безпечна речовина для переробки харчових продуктів за умови дотримання встановлених стандартів.
-У м'ясних продуктах він використовується як антимікробний засіб, здатний усувати бактерії, такі як E. coli, зменшуючи його до невизначених рівнів. Бактерія зустрічається в кишечнику великої рогатої худоби, пристосовуючись до кислотної середовищі. Гідроксид амонію, регулюючи рН, перешкоджає росту бактерій.
Терапевтичні засоби
-Гідроксид амонію має кілька терапевтичних застосувань, включаючи:
-10% розчин використовують як респіраторний рефлекторний стимулятор
-Зовнішньо він використовується на шкірі для лікування укусів комах і укусів - Він діє на травну систему як антацидний і вітрогінний, тобто він допомагає усуненню газів.
Крім того, він застосовується як топічний рубефациент для гострої та хронічної опорно-рухової болю. Внаслідок рубераційного дії гідроксиду амонію відбувається місцеве підвищення кровотоку, почервоніння і подразнення.
Промислове та інше
-Він діє у відношенні NOx (високореактивні гази, такі як оксид азоту (NO) та діоксид азоту (NO)2)) для викидів штабеля та зменшення викидів NOx у викидах димоходу.
-Використовується як пластифікатор; Добавка фарб і для обробки поверхонь.
-Це підвищує пористість волосся, дозволяючи пігментам плями мати більше проникнення, що забезпечує кращу обробку.
-Гідроксид амонію використовується як антимікробний засіб при очищенні стічних вод. Крім того, вона втручається в синтез хлораміну. Ця речовина виконує функцію, подібну до хлору при очищенні води плавального басейну, що має перевагу, що є менш токсичним.
-Використовується як інгібітор корозії в процесі переробки нафти.
-Використовується в якості очищувального засобу в різних промислових і комерційних продуктах, застосовується на декількох поверхнях, включаючи: нержавіючу сталь, фарфор, скло та піч.
-Крім того, він використовується у виробництві миючих засобів, мила, фармацевтичних препаратів і фарб.
У сільському господарстві
Хоча гідроксид амонію безпосередньо не вводиться як добриво, він виконує цю функцію. Аміак виробляють з атмосферного азоту методом Хабера-Боша і транспортують охолодженим нижче точки кипіння (-33 ° С) до місць його використання.
Аміак, що знаходиться під тиском, вводять у водяну форму в ґрунт, де він негайно реагує з едафічною водою і переходить у форму амонію (NH)4+), яка зберігається в місцях обміну катіонів грунту. Крім того, отримують гідроксид амонію. Ці сполуки є джерелом азоту.
Разом з фосфором і калієм азот є тріадою основних поживних речовин рослин, необхідних для його росту.
Список літератури
- Ganong, W. F. (2002) Медична фізіологія. 19-е видання. Редакційне сучасне керівництво.
- A. Fortes, J. P. Brodholt, І. G. Wood, і L. Vocadlo. (2001). Ab initio моделювання моногідрату аміаку (NH3. H2O) і гідроксид амонію (NH4OH). Американський інститут фізики. J. Chem., Phys., Том 115, № 15, 15.
- Helmenstine, Anne Marie, Ph.D. (6 лютого 2017 року). Факти гідроксиду амонію. Отримано з: thoughtco.com
- Група Pochteca. (2015). Гідроксид амонію. pochteca.com.mx
- NJ Здоров'я (s.f.). Інформаційний бюлетень про небезпечні речовини: гідроксид амонію. [PDF] Отримано з: nj.gov
- Учнів з хімії. (2018). Гідроксид амонію. Отримано з: chemistrylearner.com
- PubChem. (2018). Гідроксид амонію. Отримано з: pubchem.ncbi.nlm.nih.gov


