Процес екзотермічної реакції, типи і приклади
The екзотермічна реакція є типом хімічної реакції, при якій відбувається передача енергії, головним чином у вигляді виділення тепла або світла. Назва походить від грецького префікса exo, що означає "за кордоном"; і термін "термічний", який відноситься до тепла або температури.
У цьому сенсі екзотермічні реакції можуть передавати інші види енергії в навколишнє середовище, де вони генеруються, наприклад, при вибухах і способі передачі кінетичної і звукової енергії, коли речовини, що знаходяться в газовій фазі при високих температурах, розширюються. насильницьким шляхом.
Так само, у випадку використання батарей, також проводиться екзотермічна реакція, тільки в цьому випадку електрична енергія транспортується.
Індекс
- 1 Процес
- 2 типи
- 2.1 Реакції горіння
- 2.2 Реакції нейтралізації
- 2.3 Реакції окислення
- 2.4 Реакція термітів
- 2.5 Реакційна полімеризація
- 2.6 Реакція ядерного поділу
- 2.7 Інші реакції
- 3 Приклади
- 4 Посилання
Процес
Раніше було згадано, що коли відбувається екзотермічна реакція, відбувається вивільнення енергії, яка може бути легше візуалізована в наступному рівнянні:
Реагенти (и) → Продукт (и) + Енергія
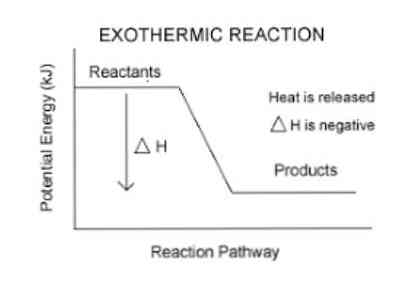
Отже, для кількісної оцінки енергії, поглиненої або вивільненої системою, використовується термодинамічний параметр, що називається ентальпією (позначений "H"). Якщо в системі (в даному випадку хімічна реакція) відбувається виділення енергії в навколишнє середовище, то зміна ентальпії (виражена як ΔH) буде мати від'ємне значення.
В іншому випадку, якщо зміна цього показника є позитивною, вона відображає поглинання тепла з оточення. Крім того, величина зміни ентальпії системи є вираженням кількості енергії, яка передається в або з навколишнього середовища.
Чим більше величина ΔH, тим більше вивільнення енергії з системи на навколишнє середовище.
Це пояснюється тим, що в цих реакціях чиста енергія, яка вивільняється при створенні нових зв'язків, більше, ніж чиста енергія, що використовується при фрагментації ланок.
З вищевикладеного можна зробити висновок, що цей вид реакцій є дуже поширеним, оскільки продукти реакції мають кількість енергії, що зберігається в зв'язках, що більше, ніж міститься в реагентах..
Типи
Існують різні види екзотермічних реакцій в різних областях хімії, будь то в лабораторії або в промисловості; деякі з них здійснюються спонтанно, а іншим потрібні конкретні умови або якийсь тип речовини, наприклад, каталізатор.
Нижче наведені найбільш важливі типи екзотермічних реакцій:
Реакції горіння
Реакції горіння є реакціями окислювально-відновного типу, які відбуваються, коли одне або кілька речовин вступають у реакцію з киснем, як правило, призводять до вивільнення світла і теплової енергії, тобто світла і тепла, коли виробляється полум'я..
Реакції нейтралізації
Реакції нейтралізації характеризуються взаємодією між кислотним видом і лужною речовиною (основою) для утворення солі і води, які проявляють екзотермічну природу.
Реакції окислення
Існує безліч реакцій цього типу, які проявляють екзотермічну поведінку, оскільки окислення кисню викликає виділення великої кількості енергії, як це відбувається при окисленні вуглеводнів..
Реакція термітів
Ця реакція може виробляти температуру приблизно 3000 ° С, і внаслідок високої спорідненості порошку алюмінію з великою кількістю оксидів металів, вона використовується при зварюванні сталі і чавуну..
Реакція полімеризації
Цей тип реакції є тим, що виникає тоді, коли реагує певна кількість хімічних речовин, званих мономерами, які є об'єктами, які при комбінуванні повторюються в ланцюгах, утворюючи макромолекулярні структури, звані полімерами.
Реакція ядерного поділу
Цей процес відноситься до поділу ядра атома, який вважається важким - тобто з масовим числом (А) більше 200 - для отримання фрагментів або ядер меншого розміру з проміжною масою.
У цій реакції, де утворюється один або більше нейтронів, виділяється велика кількість енергії, оскільки серцевина з більшою вагою має меншу стабільність, ніж її продукти.
Інші реакції
Існують також інші екзотермічні реакції, що мають велике значення, такі як дегідратація деяких вуглеводів при взаємодії з сірчаною кислотою, поглинання води, яка має гідроксид натрію під впливом відкритого повітря або окислення видів металів у багатьох корозійних реакціях..
Приклади
Нижче наведені деякі приклади екзотермічних реакцій, які виробляють зміну ентальпії, що має негативне значення внаслідок того, що вони вивільняють енергію, як згадувалося вище..
Наприклад, спалювання пропану є спонтанною екзотермічною реакцією:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Інший випадок екзотермічної поведінки проявляється реакцією нейтралізації між карбонатом натрію і соляною кислотою:
NaHCO3(ac) + HCl (ac) → NaCl (ac) + H2O (l) + CO2(g)
Представлено також окислення етанолу до оцтової кислоти, що використовується в аеродинаміках, повна реакція якої показана в наступному рівнянні:
3CH3CH2OH + 2K2Cr2O7 + 8H2SO4 → CH3COOH + 2Cr (SO4)3 + 2K2SO4 + 11H2O
Іншим класом екзотермічної реакції є так звана термітна реакція, в якій алюміній об'єднується з оксидом металу, як показано нижче:
2Al (s) + Віра2O3(s) → Al2O3(s) + Fe (l)
На додаток до наведених вище прикладів існує широкий спектр реакцій, які також вважаються екзотермічними, такими як розкладання деяких органічних відходів речовин для компостування..
Вона також підкреслює окислення люциферинового пігменту дією ферменту люциферази для отримання біолюмінесценції, характерної для світлячків, і навіть дихання, серед багатьох інших реакцій.
Список літератури
- Вікіпедія. (s.f.). Екзотермічна реакція. Отримано з es.wikipedia.org
- BBC (s.f.). Зміни енергії та оборотні реакції. Отримано з bbc.co.uk
- Chang, R. (2007). Хімія, дев'яте видання. (McGraw-Hill).
- Уокер, Д. (2007). Хімічні реакції. Отримано з books.google.co.ve
- Saunders, N. (2007). Дослідження хімічних реакцій. Отримано з books.google.co.ve


