Структура, властивості та використання оксиду кальцію (CaO)
The оксид кальцію (CaO) - неорганічна сполука, яка містить кальцій і кисень в іонних формах (не слід плутати з пероксидом кальцію, CaO)2). Він відомий у всьому світі як вапно, слово, яке позначає будь-яку неорганічну сполуку, що містить карбонати, оксиди кальцію і гідроксиди, а також інші метали, такі як кремній, алюміній і залізо..
Цей оксид (або вапно) також розмовно називають негашеним вапном або гашеною вапном, залежно від того, чи він є гідратованим. Вапном є оксид кальцію, а гашене вапно - його гідроксид. У свою чергу, вапняк (вапняний камінь або загартований вапно) фактично є осадовою породою, що складається в основному з карбонату кальцію (CaCO).3).

Це один з найбільших природних джерел кальцію і є сировиною для виробництва оксиду кальцію. Як виробляється цей оксид? Карбонати чутливі до термічного розкладання; нагрівання карбонатів кальцію при температурі вище 825 ° С, що призводить до утворення вапна і діоксиду вуглецю.
Вищенаведене твердження можна описати наступним чином: CaCO3(s) → CaO (s) + CO2(g) Оскільки земна кора багата вапняком і кальцитом, а в океанах і пляжах є багато морських раковин (сировина для виробництва оксиду кальцію), оксид кальцію відносно дешевий реагент.
Індекс
- 1 Формула
- 2 Структура
- 3 Властивості
- 3.1 Розчинність
- 4 Використання
- 4.1 Як розчин
- 4.2 У виробництві склянок
- 4.3
- 4.4 В якості силікатного засобу для видалення
- 5 Наночастинки оксиду кальцію
- 6 Посилання
Формула
Хімічною формулою оксиду кальцію є CaO, в якій кальцій нагадує іон кислоти (акцептор електронів) Ca2+, і кисню в якості основного іона (донора електронів) OR2--.
Чому кальцій має +2 заряд? Оскільки кальцій належить до групи 2 періодичної таблиці (р-н Бекамбара), і є тільки два валентних електрона, доступні для утворення зв'язків, які дають атом кисню..
Структура
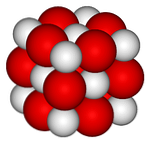
На верхньому зображенні представлена кристалічна структура (тип гем-солі) для оксиду кальцію. Об'ємні червоні сфери відповідають іонам Са2+ і білі сфери до іонів O2-.
У цьому кубічному розташуванні кристалів кожен іон Ca2+ оточений шістьма іонами O2-, закупорювалися в октаедричні отвори, що залишаються великими іонами між ними.
Ця структура максимально виражає іонний характер цього оксиду, хоча помітна різниця радіусів (червона сфера більше, ніж біла) надає більш слабку кристалічну ретикулярну енергію в порівнянні з MgO.
Властивості
Фізично це кристалічна біла тверда речовина, без запаху і з сильними електростатичними взаємодіями, які відповідають за високі точки плавлення (2572 ° C) і кипіння (2850 ° C). Крім того, вона має молекулярну масу 55,958 г / моль і цікаву властивість бути термолюмінесцентними.
Це означає, що шматочок оксиду кальцію, який піддається полум'я, може світитися інтенсивним білим світлом, відомий англійською мовою з назвою в центрі уваги, або іспанською, світло кальцію. Іони Са2+, при контакті з вогнем вони викликають червоне полум'я, як показано на наступному зображенні.

Розчинність
CaO являє собою основний оксид, який має сильну спорідненість до води, в тій мірі, в якій він поглинає вологу (він є гігроскопічним твердим речовиною), реагуючи негайно для отримання гашеного вапна або гідроксиду кальцію:
CaO (s) + H2O (l) => Ca (OH)2s
Ця реакція є екзотермічною (виділяє тепло) за рахунок утворення твердої речовини з більш сильними взаємодіями і більш стабільною кристалічної решіткою. Однак реакція оборотна, якщо нагріти Ca (OH)2, зневоднення і освітлення гашеної вапна; тоді, вапно "перероджується".
Отриманий розчин дуже основний, і якщо він насичений оксидом кальцію, він досягає рН 12,8.
Крім того, він розчинний у гліцерині, а також у кислотних і цукрових розчинах. Оскільки вона є основним оксидом, вона, природно, має ефективні взаємодії з оксидами кислот (SiO2, Al2O3 і Віра2O3, наприклад, розчинний у рідких фазах. З іншого боку, він нерозчинний у спиртах і органічних розчинниках.
Використання
CaO має величезну кількість промислових застосувань, а також у синтезі ацетилену (CH ,CH), в екстракції фосфатів з стічних вод і в реакції з діоксидом сірки з газоподібних відходів..
Інші способи використання оксиду кальцію описані нижче:
Як розчин
Якщо оксид кальцію змішується з піском (SiO2) і воду, пиріжки з піском і повільно реагує з водою з утворенням гашеного вапна. У свою чергу СО2 повітря розчиняється у воді і вступає в реакцію з сіллю, утворюючи карбонат кальцію:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2O (l)
CaCO3 Це більш стійка і твердіша сполука, ніж CaO, що призводить до того, що розчин (попередня суміш) затвердіє і закріплює цеглини, блоки або кераміку між ними або на бажану поверхню.
У виробництві стекол
Істотною сировиною для виробництва склянок є оксиди кремнію, які змішуються з вапном, карбонатом натрію (Na2CO3) та інших добавок, які потім піддають нагріванню, в результаті чого утворюється склоподібне тверда речовина. Дане тверда речовина згодом нагрівається і продувається будь-якими фігурами.
У гірничій справі
Гашене вапно займає більший об'єм, ніж негашене вапно внаслідок взаємодії водневих зв'язків (O-H-O). Ця властивість використовується для розриву порід зсередини.
Це досягається шляхом заповнення їх компактною сумішшю вапна і води, яка запечатана, щоб зосередити свою теплоту і експансивну потужність в скелі..
Як силікатне видалення
CaO зливається з силікатами з утворенням коалесцентної рідини, яка потім витягується з сировини певного продукту.
Наприклад, залізні руди є сировиною для виробництва металевого чавуну і сталі. Ці мінерали містять силікати, які є небажаними домішками для процесу і усуваються тільки описаним способом.
Наночастинки оксиду кальцію
Оксид кальцію може бути синтезований у вигляді наночастинок, що змінюють концентрації нітрату кальцію (Ca (NO)3)2) і гідроксид натрію (NaOH) в розчині.
Ці частинки сферичні, основні (як і макромасштабні тверді) і мають велику площу поверхні. Отже, ці властивості сприяють каталітичним процесам. Які? В даний час розслідування відповідають на це питання.
Ці наночастинки використовувалися для синтезу заміщених органічних сполук, отриманих з піридинів, у формулюванні нових препаратів для проведення хімічних перетворень, таких як штучний фотосинтез, для очищення води від важких і шкідливих металів, а також фотокаталітичні агенти.
Наночастинки можуть бути синтезовані на біологічній основі, такі як листя папайї і зеленого чаю, які використовуються як антибактеріальний засіб.
Список літератури
- scifun.org (2018). Вапно: оксид кальцію. Отримано 30 березня 2018 р. З: scifun.org.
- Вікіпедія. (2018). Оксид кальцію. Отримано 30 березня 2018 року з: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). Зелений синтез наночастинок оксиду кальцію та його застосування. Міжнародний журнал інженерних досліджень та застосування. ISSN: 2248-9622, т. 6, випуск 10, (Частина -1), с.27-31.
- J. Safaei-Ghomi et al. (2013). Наночастинки оксиду кальцію каталізуються одностадійним багатокомпонентним синтезом високозаміщених піридинів у водному середовищі етанолу Scientia Iranica, Transactions C: Хімія та хімічна промисловість 20 549-554.
- PubChem. (2018). Оксид кальцію. Отримано 30 березня 2018 року з: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Неорганічна хімія В Елементи групи 2. (четверте видання, стор. 280). Mc Graw Hill.


