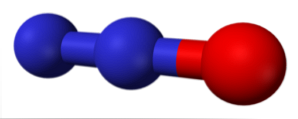
Оксиди азоту (NOx) Різні склади та номенклатури
The оксиди азоту вони є по суті газоподібними неорганічними сполуками, які містять зв'язки між атомами азоту і кисню. Її групова хімічна формула НІx, що вказує на те, що оксиди мають різні пропорції кисню і азоту.
Азот веде групу 15 періодичної таблиці, тоді як киснева група 16; обидва елементи є членами періоду 2. Ця близькість є причиною, чому N-O зв'язки ковалентні в оксидах. Таким чином, зв'язки в оксидах азоту є ковалентними.
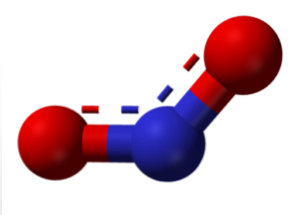
Всі ці зв'язки можна пояснити, використовуючи теорію молекулярної орбіталі, яка виявляє парамагнетизм (електрон, неспарений в останній молекулярній орбіталі) деяких з цих сполук. З них найбільш поширеними сполуками є оксид азоту і діоксид азоту.
Молекула у верхньому зображенні відповідає кутовій структурі в газовій фазі діоксиду азоту (NO2). Навпаки, оксид азоту (NO) має лінійну структуру (враховуючи sp-гібридизацію для обох атомів).
Оксиди азоту - це гази, що утворюються при багатьох видах діяльності людини, від водіння автомобіля або куріння сигарет, до промислових процесів, що забруднюють відходи. Проте NO природно утворюється в результаті ферментативних реакцій і блискавок у грозах: N2(g) + O2(g) => 2NO (g)
Високі температури променів розривають енергетичний бар'єр, що запобігає виникненню цієї реакції в нормальних умовах. Який енергетичний бар'єр? Що утворюється потрійним зв'язком N≡N, що робить N-молекулу2 інертний газ з атмосфери.
Індекс
- 1 Номери окиснення азоту та кисню в їх оксидах
- 2 Різні формулювання та номенклатури
- 2.1 Закис азоту (N2O)
- 2.2 Оксид азоту (NO)
- 2.3 Триоксид азоту (N2O3)
- 2.4 Двоокис і тетраоксид азоту (NO2, N2O4)
- Пентаоксид динітрогену (N2O5)
- 3 Посилання
Номери окислення азоту і кисню в їх оксидах
Електронна конфігурація для кисню [He] 2s22p4, потребують лише двох електронів для завершення октету своєї валентної оболонки; тобто, він може отримати два електрона і мати кількість окислення, що дорівнює -2.
З іншого боку, електронна конфігурація для азоту [He] 2s22p3, здатність отримати до трьох електронів, щоб заповнити його валентний октет; наприклад, у разі аміаку (NH3) має кількість окислення, рівне -3. Але кисень набагато більш електронегативний, ніж водень, і «змушує» азот ділитися своїми електронами.
Скільки електронів може розділити азот з киснем? Якщо ви розділяєте електрони вашої валентної оболонки один за одним, ви досягнете межі п'яти електронів, що відповідає кількості окислення +5.
Отже, в залежності від того, скільки зв'язків він утворює з киснем, кількість окислення азоту коливається від +1 до +5.
Різні формулювання та номенклатури
Оксиди азоту, в порядку збільшення кількості окислювальних азоту, становлять:
- N2Або, закис азоту (+1)
- NO, оксид азоту (+2)
- N2O3, триоксид азоту (+3)
- NO2, діоксид азоту (+4)
- N2O5, пентоксид азоту (+5)
Закис азоту (N2O)
Закис азоту (або в народі відомий як газ для сміху) являє собою безбарвний газ з легким солодким запахом і мало реагує. Він може бути візуалізований як молекула N2 (сині сфери), що додав атом кисню на одному кінці. Його готують шляхом термічного розкладання нітратних солей і використовують як знеболюючий і знеболюючий засіб.
Азот має кількість окислення +1 в цьому оксиді, що означає, що він не дуже окислюється і його потреба в електронах не є переконливою; однак, потрібно лише отримати два електрони (по одному для кожного азоту), щоб стати стабільним молекулярним азотом.
У основних і кислотних розчинах реакції:
N2O (g) + 2H+(ac) + 2e- => N2(g) + H2O (l)
N2O (g) + H2O (l) + 2e- => N2(g) + 2OH-(ac)
Ці реакції, хоча і термодинамічно, сприяють утворенню стійкої молекули N2, протікають повільно і реагенти, які дарують пару електронів, повинні бути дуже сильними відновлюючими агентами.
Оксид азоту (NO)
Цей оксид складається з безбарвного, реактивного і парамагнітного газу. Як і закис азоту, вона має лінійну молекулярну структуру, але з великою різницею в тому, що зв'язок N = O також має характер потрійного зв'язку..
NO швидко окислюється в повітрі з утворенням NO2, і таким чином генерувати більш стабільні молекулярні орбіталі з більш окисленим атомом азоту (+4).
2NO (g) + O2(g) => 2NO2(g)
Біохімічні та фізіологічні дослідження стоять за доброякісною роллю цього оксиду в живих організмах.
Вона не може утворювати N-N зв'язки з іншою молекулою NO через ділокалізацію непарного електрона в молекулярній орбіталі, яка спрямована більше на атом кисню (завдяки високій електронегативності). Протилежне відбувається з NO2, які можуть утворювати газоподібні димери.
Триоксид азоту (N2O3)
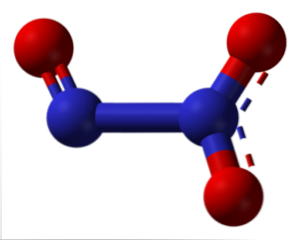
Пунктирні лінії структури вказують на подвійний резонанс зв'язку. Як і всі атоми, вони мають sp-гібридизацію2, молекула є плоскою і молекулярні взаємодії є достатньо ефективними для існування триоксиду азоту у вигляді синьої твердої речовини нижче -101ºC. При більш високих температурах вона плавиться і дисоціюється на NO і NO2.
Чому вона відокремлена? Оскільки числа окислення +2 і +4 є більш стабільними, ніж +3, останні присутні в оксиді для кожного з двох атомів азоту. Це, знову ж таки, можна пояснити стабільністю молекулярних орбіталей, що є результатом диспропорції.
На зображенні ліва сторона N2O3 відповідає NO, тоді як права сторона NO2. Логічно, що воно утворюється при коалесценції попередніх оксидів при дуже низьких температурах (-20ºC). N2O3 є ангідридом азотистої кислоти (HNO2).
Двоокис і тетроксид азоту (NO2, N2O4)
NO2 це коричневий або коричневий газ, реактивний і парамагнітний. Оскільки вона має непарний електрон, вона димеризується (зв'язується) з іншою газоподібною молекулою NO2 утворити азотний тетроксид, безбарвний газ, що встановлює баланс між обома хімічними видами:
2NO2(g) <=> N2O4(g)
Він є отруйним і універсальним окислювачем, здатним диспропорционировать його окисно-відновні реакції в іонах (оксоанионах).2- і NO3- (генерування кислотних дощів) або в NO.
Аналогічно, NO2 бере участь у складних атмосферних реакціях, що викликають зміни концентрацій озону (OR3) на земних рівнях і в стратосфері.
Пентаоксид азоту (N2O5)
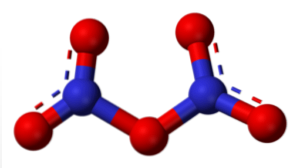
При гідратації він генерує HNO3, і при більш високих концентраціях кислоти кисень переважно протонируется з частковим позитивним зарядом -О+-Н, прискорення окисно-відновних реакцій
Список літератури
- ініціанти. ((2006-2018)). ініціанти. Отримано 29 березня 2018 р. Від анкетиііті: askiitians.com
- Encyclopaedia Britannica, Inc. (2018). Енциклопедія Британіка. Отримано 29 березня 2018 р. З Encyclopaedia Britannica: britannica.com
- Tox Town. (2017). Tox Town. Отримано 29 березня 2018 р. З Tox Town: toxtown.nlm.nih.gov
- Професор Патрісія Шаплі. (2010). Оксиди азоту в атмосфері. Університет Іллінойсу. Отримано 29 березня 2018 року від: butane.chem.uiuc.edu
- Shiver & Atkins. (2008). Неорганічна хімія В Елементи групи 15. (Четверте видання., С. 361-366). Mc Graw Hill