Бутіно структура, властивості і застосування
The butino являє собою хімічну сполуку, що належить до групи алкінів, що характеризується, головним чином, наявністю у своїй структурі, щонайменше, потрійного зв'язку між двома атомами вуглецю.
Коли йдеться про встановлення правил для номіналу алкинов, IUPAC (акронім на англійській мові для Міжнародного союзу чистої і прикладної хімії) встановив, що вони використовуються так само, як і для алкенів.

Принципова відмінність між номенклатурою обох типів речовин полягає в тому, що суфікс -один змінюється на -або коли мова йде про сполуки, які мають потрійні зв'язки у своїй структурі.
З іншого боку, бутіно складається тільки з вуглецю і водню, і він поставляється в двох формах: 1-бутин, який знаходиться в газовій фазі при стандартних умовах тиску і температури (1 атм, 25 ° С); і 2-бутіно, який являє собою рідкофазний вид, отриманий хімічним синтезом.
Індекс
- 1 Хімічна структура
- 1.1 1-бутино
- 1.2 2-бутина
- 2 Властивості
- 3 Використання
- 4 Посилання
Хімічна структура
У молекулі, відомій як бутіно, представлено явище структурної ізомеризації положення, яке полягає в наявності однакових функціональних груп в обох сполуках, але кожна з них знаходиться в іншому місці ланцюга..
У цьому випадку обидві форми бутіно мають ідентичну молекулярну формулу; однак у 1-бутині потрійний зв'язок розташований у вуглеці №1, а в 2-бутині він знаходиться у другому. Це перетворює їх у позиційні ізомери.
Завдяки розташуванню потрійної зв'язку в одному з терміналів 1-бутінової структури вона розглядається як кінцевий алкин, тоді як проміжне положення потрійного зв'язку в 2-бутиновій структурі дає класифікацію внутрішнього алкина..
Таким чином, зв'язок може бути тільки між першим і другим вуглецем (1-бутином) або між другим і третім вуглецем (2-бутином). Це пов'язано з застосовуваною номенклатурою, де найнижча можлива нумерація завжди буде надана позиції потрійного зв'язку.
1-бутино
З'єднання під назвою 1-бутин також відоме як етилацетилен, тому що його структура і спосіб, в якому його розташовані і скріплені його чотири атома вуглецю. Однак, коли йдеться про butino Посилання робиться тільки на цей хімічний вид.
У цій молекулі потрійний зв'язок знаходиться в кінцевому вуглеці, що дозволяє забезпечити наявність атомів водню, які надають йому велику реактивність.
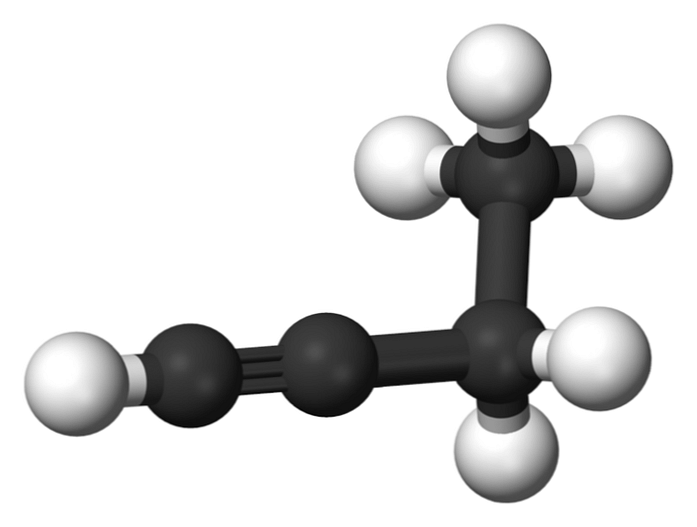
Ця жорстка і більш міцна зв'язок, ніж єдина або подвійна зв'язок між атомами вуглецю, забезпечує стабільну конфігурацію 1-бутинової лінійної геометрії.
З іншого боку, це газоподібне речовина досить вогненебезпечне, тому в присутності тепла вона може легко викликати пожежі або вибухи і має велику реактивність у присутності повітря або води.
2-бутина
Оскільки внутрішні алкіни демонструють більшу стабільність, ніж термінальні алкіни, вони дозволяють перетворити 1-бутин на 2-бутин.
Ця ізомеризація може відбуватися шляхом нагрівання 1-бутину в присутності підстави (наприклад, NaOH, KOH, NaOCH3 ...) або шляхом перегрупування 1-бутина в розчин гідроксиду калію (КОН) в етанолі (C).2H6O).
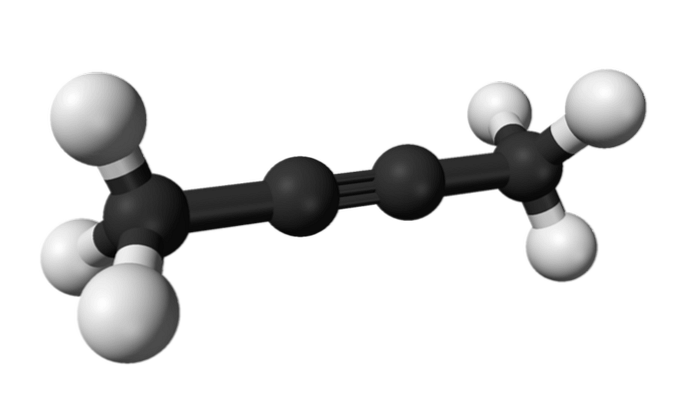
Таким же чином, хімічна речовина, відома як 2-бутин, також називається диметилацетиленом (або кротоніленом), що представляє собою рідкий і летючий вид, який походить з штучного.
У 2-бутині потрійний зв'язок знаходиться в середині молекули, що надає йому більшу стабільність, ніж її ізомер.
Крім того, ця безбарвна сполука має більш низьку щільність, ніж вода, хоча вона вважається нерозчинною в ній і має високу займистість.
Властивості
-Структурна формула бутино (незалежно від того, на який ізомер посилаються) - це C4H6, яка має лінійну структуру.
-Однією з хімічних реакцій молекули бутину є ізомеризація, в якій відбувається перегрупування і міграція потрійного зв'язку в молекулі.
-1-бутина знаходиться в газовій фазі, має дуже високу займистість і більш високу щільність, ніж повітря.
-Ця речовина також досить реакційноздатна, і при наявності тепла може викликати бурхливі вибухи.
-Крім того, коли цей безбарвний газ відчуває неповну реакцію згоряння, він може викликати окис вуглецю (CO)
-Коли обидва ізомеру піддаються впливу високих температур, вони можуть зазнати реакцій полімеризації вибухового типу.
-2-бутин знаходиться в рідкій фазі, хоча він також вважається досить легкозаймистим при стандартних умовах тиску і температури.
-Ці речовини можуть зазнавати бурхливих реакцій, коли вони знаходяться в присутності сильних окислювальних речовин.
-Таким же чином екзотермічні реакції з подальшим вивільненням газоподібного водню відбуваються при наявності відновлювальних видів..
-При виявленні в контакті з певними каталізаторами (такими як деякі кислотні речовини) або видів закваски можуть відбуватися реакції полімеризації екзотермічного типу..
Використання
Оскільки вони мають деякі різні властивості, обидва ізомери можуть мати різні застосування і застосування, як показано нижче:
По-перше, дуже часто одним із застосувань 1-бутіно є його використання як проміжної стадії у процесі виробництва інших речовин органічної природи синтетичного походження..
З іншого боку, цей хімічний вид використовується в обробній промисловості гумових і похідних сполук; як, наприклад, коли потрібно отримати бензол.
Аналогічно, він використовується в процесі виготовлення широкого спектру пластмасових виробів, а також у виробництві багатьох поліетиленових речовин, які вважаються високою щільністю.
Також 1-бутин часто використовується як компонент для різання і зварювання деяких металевих сплавів, включаючи сталь (сплав заліза і вуглець)..
В іншому сенсі, 2-бутиновий ізомер використовується в комбінації з іншим алкином, який називається пропіном в синтезі деяких речовин, відомих як алкілірованние гідрохінони, коли проводиться процес тотального синтезу α-токоферолу (вітаміну Е)..
Список літератури
- Вікіпедія. (s.f.). Бутине Отримано з en.wikipedia.org
- Yoder, C.H., Leber P.A. і Thomsen, M.W. (2010). Міст до органічної хімії: поняття та номенклатура. Отримано з books.google.co.ve
- Study.com. (s.f.). Бутини: Структурна формула та ізомери. Отримано з дослідження.
- PubChem. (s.f.). 1-Бутину. Отримано з pubchem.ncbi.nlm.nih.gov
- PubChem. (s.f.). 2-Бутину. Отримано з pubchem.ncbi.nlm.nih.gov


