Формула пропанової кислоти, властивості, ризики та застосування
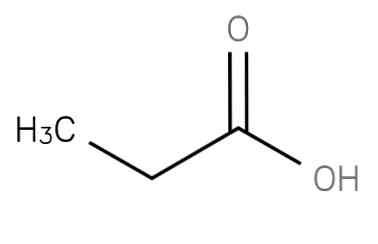
The пропанової кислоти являє собою насичену коротколанцюгову жирну кислоту, що містить етан, приєднаний до вуглецю карбокси групи. Його формула - CH3-CH2-COOH. Аніон CH3CH2COO-, а також солі і складні ефіри пропанової кислоти відомі як пропіонати (або пропаноати).
Він може бути отриманий з відходів деревної маси шляхом процесу ферментації з використанням бактерій роду propionibacterium. Він також отримують з етанолу і монооксиду вуглецю з використанням каталізатора трифториду бору (O'Neil, 2001).
Іншим способом отримання пропанової кислоти є окислення пропиональдегида в присутності іонів кобальту або марганцю. Ця реакція швидко розвивається при температурах до 40-50 ° C:
2CH3CH2CHO + O2 → 2CH3CH2COOH
З'єднання природно присутня на низькому рівні в молочних продуктах і виробляється в загальному вигляді, поряд з іншими жирними кислотами з коротким ланцюгом, в шлунково-кишковому тракті людини та інших ссавців як кінцевий продукт мікробного перетравлення вуглеводів..
Має значну фізіологічну активність у тварин (База даних метаболомів людини, 2017).
Індекс
- 1 Фізико-хімічні властивості
- 2 Реактивність і небезпека
- 3 Біохімія
- 4 Використання
- 5 Посилання
Фізико-хімічні властивості
Пропанова кислота - безбарвна і масляниста рідина з їдким, неприємним і прогорілим запахом. Його вигляд показаний на малюнку 2 (Національний центр інформації про біотехнології, 2017).

Пропанова кислота має молекулярну масу 74,08 г / моль і щільність 0,992 г / мл. Його точка замерзання і температура кипіння становлять -20,5 ° C і 141,1 ° C відповідно. Пропанова кислота є слабкою кислотою, pKa якої становить 4,88.
З'єднання дуже добре розчиняється у воді, здатне розчиняти 34,97 г з'єднання на 100 мл розчинника. Він також розчинний у етанолі, ефірі та хлороформі (Royal Society of Chemistry, 2015).
Пропанова кислота має проміжні фізичні властивості між тими, що містять менші карбонові кислоти, мурашину та оцтову кислоти, і більші жирні кислоти.
Він показує загальні властивості карбонових кислот і може утворювати амідні, складні ефірні, ангідридні та хлоридні похідні. Він може піддаватися альфа-галогенированию бромом у присутності PBr3 в якості каталізатора (реакція HVZ) з утворенням CH3CHBrCOOH.
Реактивність і небезпека
Пропанова кислота є горючим і горючим матеріалом. Вона може запалюватися теплом, іскрою або полум'ям. Пари можуть утворювати вибухонебезпечні суміші з повітрям, здатні проїхати до джерела запалювання і вибухнути.
Більшість парів важче повітря. Вони будуть поширюватися по землі і збиратимуться в низьких або закритих зонах (каналізація, підвали, резервуари). Небезпека вибуху пари в приміщенні, на відкритому повітрі або в каналізаціях.
Речовини, позначені a (P), можуть полімеризуватися вибухово, коли вони нагріваються або обгортаються у вогні. Контейнери можуть вибухнути при нагріванні (PROPIONIC ACID, 2016).
З'єднання слід зберігати подалі від тепла або джерел займання. При нагріванні до розкладання виділяється гострий дим і подразнюючі пари.
Пропанова кислота подразнює шкіру, очі, ніс і горло, але не дає гострих системних ефектів і не має очевидного генотоксичного потенціалу. У разі контакту слід промити великою кількістю води (Паспорт безпеки пропіонової кислоти, 2013).
Біохімія
Кон'югатна основа пропанової кислоти, пропіонату, утворюється як кінцевий фрагмент з трьох вуглецевих атомів (активованих коферментом А як пропионил-КоА) при окисленні непарних жирних кислот вуглецю і окислення бічного ланцюга холестерину.
Експерименти з радіоактивними ізотопами пропіонату, що вводяться на щурячих щурах, свідчать про те, що він може з'являтися в глікогені, глюкозі, проміжних продуктах циклу лимонної кислоти, амінокислотах і білках.
Шлях метаболізму пропанової кислоти включає взаємодію з коферментом А, карбоксилювання з утворенням метилмалоніл-коферменту А і перетворення в янтарну кислоту, яка надходить у цикл лимонної кислоти..
Пропанова кислота може бути окислена без утворення кетонових тіл і, на відміну від оцтової кислоти, включена в вуглевод, а також ліпід (Bingham, Cohrssen, & Powell, 2001).
Пропіонова кислота є однією з найбільш частих органічних кислот, хвороба, що включає багато різноманітних розладів.
Результати пацієнтів, народжених з пропіонової ацетурією, мають низький рівень інтелектуального розвитку, 60% мають IQ менше 75 і потребують спеціальної освіти..
Успішні трансплантації печінки та / або нирок у декількох пацієнтів призвели до поліпшення якості життя, але не обов'язково запобігли неврологічним та вісцеральним ускладненням.
Ці результати підкреслюють необхідність постійного метаболічного моніторингу, незалежно від терапевтичної стратегії.
Використання
Пропанова кислота пригнічує ріст бактерій і цвілі на рівні від 0,1 до 1% по масі. Як наслідок, більша частина виробленої пропанової кислоти споживається як консервант як для кормів, так і для харчових продуктів для споживання людиною, таких як зернові та зернові культури..
Збереження кормів, зернових та харчових продуктів, а також виробництво пропіонату кальцію і натрію, що становить майже 80% світового споживання пропанової кислоти у 2016 році, порівняно з 78,5% у 2012 році.
Приблизно 51% світового споживання пропанової кислоти використовується для комбікормів та збереження зерна, а майже 29% - для виробництва пропіонатів кальцію та натрію, які також використовуються у харчовій та кормовій промисловості..
Іншими важливими ринками для пропанової кислоти є виробництво гербіцидів та дієтилового кетону. Застосування з меншим об'ємом включає пропіонат целюлози, фармацевтичні препарати, ефіри розчинників, ароматизатори та ароматизатори, пластифікатори, барвники та текстильні допоміжні засоби, шкіру та гуму.
Попит на пропанову кислоту значною мірою залежить від виробництва комбікормів та зернових, а також упакованих продуктів та хлібобулочних виробів..
Перспективи глобального зростання пропанової кислоти та її солей у тваринництві / зерні та збереженні харчових продуктів є значними (IHS Markit, 2016).
Інші швидко зростаючі ринки включають ефіри пропіонату для розчинників, такі як н-бутил пропіонат і пентил; Ці складні ефіри все частіше використовуються в якості замінників розчинників, зазначених як небезпечні забруднювачі повітря.
Список літератури
- Bingham, E., Cohrssen, B., & Powell, C. (2001). Томічність томів Патті 1-9 5-е изд. Нью-Йорк: Джон Віллі та сини.
- EMBL-EBI (2016, 14 жовтня). пропіонова кислота. Відновлюється від ChEBI: ebi.ac.uk.
- Метаболом людини бази даних. (2017, 2 березня). Пропіонова кислота. Отримано з hmdb.ca: hmdb.ca.
- IHS Markit. (2016, грудень). Підручник з хімічної економіки Пропіонова кислота. Отримано з ihs: ihs.com.
- Паспорт безпеки матеріалу Пропіонова кислота. (2013, 21 травня). Отримано з sciencelab: sciencelab.com.
- Національний центр біотехнологічної інформації ... (2017, 22 квітня). База даних PubChem Compound; CID = 1032. Отримано з pubchem.ncbi.nlm.nih.gov.
- O'Neil, M. (. (2001), Індекс Merck - Енциклопедія хімічних речовин, наркотиків і біологічних препаратів, 13-е видання, Нью-Джерсі: Merck and Co., Inc..
- Пропіонова кислота. (2016). Отримано з cameochemicals: cameochemicals.noaa.gov.
- Королівське хімічне товариство. (2015). Пропіонова кислота. Отримано з chemspider: chemspider.com.


