Хлорид амонію (NH4Cl) Формула, властивості, ризики та застосування
The хлорид амонію, також відома як аміачна сіль, являє собою неорганічну сіль, виявлену в сечі, формулою якої є NH4Cl, він міститься в мінералогічних формаціях і в цій формі називається солі аміаку. Він також був знайдений у деяких вулканічних отворах і попелі.
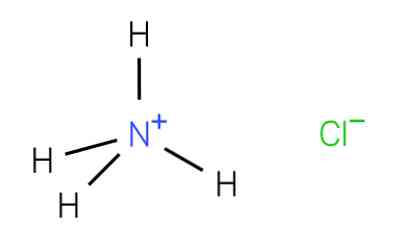
Його можна отримати різними методами. Перший через нейтралізацію HCl з аміачного залишку, що утворюється при перегонці вугілля: NH3 + HCl → NH4Cl.
Друга стратегія полягає в процесі Solvay для отримання карбонату натрію (або бікарбонату), де хлорид амонію виробляється як побічний продукт:
NH3 + CO2 + NaCl + H2O → NH4Cl + NaHCO3
У процесі Solvay бікарбонат натрію виділяють фільтруванням, а потім залишається в розчині хлорид амонію (Ammonium Chloride Formula, S.F.)..
Щорічно в Японії виробляється понад 230 тис. Тонн хлориду амонію, де він використовується в основному для внесення добрив у вирощування рису.
Однак сіль без запаху має багато інших застосувань, які включають застосування при виготовленні особистих очищувальних продуктів, піротехнічних засобів, як компонента в металургійній промисловості, медицини, як ароматизатора в харчовій промисловості і в якості електроліту в цинкових батареях. -вуглець (The Chemical Company, 2016).
Індекс
- 1 Фізико-хімічні властивості
- 2 Реактивність і небезпека
- 3 Використання
- 3.1 1- Медицина
- 3.2 2- Добриво
- 3.3 3- Металургія
- 3.4 Компонент батареї
- 3.5 5 - Обід
- 3.6 6- Інші види використання
- 4 Посилання
Фізико-хімічні властивості
Хлорид амонію є гігроскопічними, дрібнодисперсними білими частинками без запаху (Національний центр інформації з біотехнології., 2017).

З'єднання має структуру триклінової мережі з кубічною структурою, центрованою в центрі. Його молекулярна маса становить 53,490 г / моль, її щільність - 1,5274 г / мл, температура плавлення і кипіння - 338 ºC та 520 ºC.
Хлорид амонію розчинний у воді, здатний розчиняти 383,0 г з'єднання на літр розчинника. Він також розчинний у етанолі, метанолі та гліцерині і слабо розчинний у ацетоні. Він нерозчинний в органічних розчинниках, таких як етилацетат (Royal Society of Chemistry, 2015).
Амоній хлорид може піддаватися різних реакцій, що мають велике значення для хімічної та фармацевтичної промисловості. Він може розкладатися при нагріванні в соляній кислоті і аміаку:
NH4Cl → NH3 + HCl
Крім того, він може реагувати з основами, такими як гідроксид натрію або калію, щоб також виробляти аміачний газ:
NH4Cl + NaOH → NH3 + NaCl + H2O
Іншою важливою реакцією, в якій використовується хлорид аміаку, є розкладання карбонатів і бікарбонатів, утворюючи сіль і аміак:
2NH4Cl + Na2CO3 → 2NaCl + CO2 + H2O + 2NH3
Хлорид амонію вважається кислою сіллю. Отримані розчини містять помірні концентрації іонів гідронію і мають рН менше 7,0. Реакцію як кислоти нейтралізують основи.
Загалом, вони не реагують як окислювачі або відновлювачі, але така поведінка неможлива. Багато з цих сполук каталізують органічні реакції (хлорид амонію, 2016).
Реактивність і небезпека
Амоній хлорид надзвичайно отруйний і токсичний. Це викликає пошкодження органів при попаданні в їжу або тривалому впливі, а також шкідливо для очей. Вона не є вогненебезпечною і не реагує з іншими хімічними речовинами (Національний інститут охорони праці, 2014).
У разі контакту з очима слід перевірити, чи носите контактні лінзи, і негайно видаліть їх. Очі слід промити проточною водою протягом принаймні 15 хвилин, залишаючи відкриті повіки. Можна використовувати холодну воду. Мазь не повинна використовуватися для очей.
Якщо хімічна речовина контактує з одягом, видаліть її якомога швидше, захищаючи власні руки і тіло.
Помістіть жертву під душем безпеки. Якщо хімічна речовина накопичується на відкритій шкірі потерпілого, наприклад, на руках, вона обережно миє забруднену шкіру проточною водою і неабразивним милом. Можна використовувати холодну воду. Якщо подразнення зберігається, зверніться за медичною допомогою. Перед повторним використанням промийте забруднений одяг.
Якщо контакт із шкірою серйозний, його слід промити дезінфікуючим милом і покрити шкірою, забрудненою антибактеріальним кремом..
У разі інгаляції потерпілому слід дозволити відпочивати в добре провітрюваному приміщенні. Якщо інгаляція є серйозною, жертву слід якомога швидше евакуювати до безпечної зони. Ослабте щільний одяг, наприклад, комір сорочки, ремені або краватку.
Якщо потерпілому важко дихати, слід вводити кисень. Якщо потерпілий не дихає, проводиться реанімація рот в рот. Завжди беручи до уваги, що може бути небезпечно для особи, яка надає допомогу, для реанімації рот в рот, коли інгаляційний матеріал є токсичним, інфекційним або корозійним.
У разі проковтування не викликати блювоту. Ослабте щільний одяг, наприклад, нагрудники, ремені або краватки. Якщо потерпілий не дихає, виконайте реанімацію з рота в рот.
У всіх випадках слід негайно звернутися до лікаря (паспорт безпеки матеріалу хлорид амонію, 2013).
Використання
1- Медицина
Амоній хлорид має дуже важливу біохімічну функцію: він підтримує фізіологічний рН.
Як кислотна сіль, вона може допомогти виправити ситуації, в яких концентрація хлорид-іонів в плазмі низька або у випадках алкалозу крові (високий рН крові). Це може статися після блювоти, всмоктування (видалення) вмісту шлунка, застосування діуретиків (таблетки води або рідини) або при деяких захворюваннях шлунка..
Хлорид амонію також призводить до усунення надлишкових солей і води за рахунок більшого сечовипускання і викликає ацидоз у сечі (робить його більш кислим).
Амоній хлорид також використовується для зменшення набряку або збільшення маси тіла, що виникає перед менструальними періодами, а також для лікування інфекцій сечовивідних шляхів (Університет Юти, 2017).
Він є компонентом багатьох ліків від холоду та кашлю через його ефективність як відхаркувальний засіб. У ветеринарії застосовують для профілактики сечових каменів у кіз, великої рогатої худоби та овець (Encyclopædia Britannica, 2016).
2- Добриво
Амоній хлорид використовується в основному в якості джерела азоту в добривах (що відповідає 90% світового виробництва сполуки), таких як хлорамонійфосфат, переважно для рисових і пшеничних культур в Азії..
3 - Металургія
Амоній хлорид використовують як флюс при приготуванні металів для покриття оловом, гальванічним або звареним. Вона працює як флюс шляхом очищення поверхні заготовок шляхом взаємодії з оксидами металів на поверхні для утворення летючого хлориду металу..
Для цього він продається в блоках в господарських магазинах для використання в очищенні наконечника паяльника, і може бути включений в припій як флюс.
4 - компонент батареї
Хлорид амонію, NH4Cl, є компонентом сухих батарей, енергетичних резервуарів, що живлять електричні пристрої. Батареї дозволяють використовувати електрику, коли Ви не знаходитесь поблизу електричної розетки або розетки.
Для кожної батареї є три основні компоненти: катод (верхня частина щоденної батареї АА, з якої протікають електрони), анод (нижня частина батареї АА, до якої протікають електрони) і електроліт до через які електрони і іони можуть рухатися.
Коли хлорид амонію використовується в якості електроліту в батареї, він стає водною пастою і поміщається між катодом і анодом.
Хімічні реакції між катодами батареї та анодами викликають протікання електронами через пасту хлориду амонію, від катода і до анода.
Електрони проходять через металеві контакти в батарейному відсіку, що робить роботу електрообладнання (American Chemistry Council, Inc., 2005).
5- Харчування
У кількох країнах хлорид амонію під назвою аміачної солі або колоїдно-сальміаккі використовують як харчову добавку під номером E E510, зазвичай як дріжджовий поживний матеріал у виробництві хліба.
Це харчова добавка для великої рогатої худоби та інгредієнт у поживних середовищах для дріжджів та багатьох мікроорганізмів.
Амоній хлорид використовується для ароматизації темних солодощів, що називаються солоним солодким (дуже популярний у північних країнах), для випікання печива дуже хрусткою текстурою, а в Salmiakki Koskenkorva - для ароматизації.
В Індії та Пакистані вона називається "Noshader" і використовується для поліпшення свіжості бутербродів, таких як samosas і jalebi.
6- Інші види використання
Амоній хлорид можна знайти в шампуні, фарбах для волосся і відбілювачі, для миття тіла та миючого засобу, для миття обличчя, кондиціонера, миючого засобу для миття посуду, а також для масел і солей для ванн.
Амоній хлорид також використовується при травленні при виготовленні друкованих схем, таких як вогнегасник. Він також є інгредієнтом у феєрверках, вибухових речовинах і сірниках і як затверджувач в клеях на основі формальдегіду.
Список літератури
- Американська хімічна рада, Inc. (2005, травень). Амоній хлорид: допомагає забезпечити портативну електроенергію. Відновлюється від американськоїхімії: americanchemistry.com.
- Амоній хлорид. (2016). Отримано з CAMEO Chemicals: cameochemicals.noaa.gov.
- Формула хлористого амонію. (S.F.). Відновлюється від софтеху: softschools.com.
- EMBL-EBI (2016, 29 лютого). хлорид амонію. Відновлюється від ChEBI: ebi.ac.uk.
- Енциклопедія Британіка. (2016, 13 квітня). Амоній хлорид (NH4Cl). Отримано з Британської енциклопедії: britannica.com.
- Паспорт безпеки матеріалу Амоній хлорид. (2013, 21 травня). Відновлено desciencelab: sciencelab.com.
- Національний центр біотехнологічної інформації. (2017, 22 квітня). База даних PubChem Compound; CID = 25517. Отримано з PubChem: pubchem.ncbi.nlm.nih.gov.
- Королівське хімічне товариство. (2015). Амоній хлорид. Отримано з chemspider: chemspider.com.
- Хімічна компанія. (2016). Хлорид амонію. Відновлюється від thechemco: thechemco.com.
- Національний інститут охорони праці. (2014, 1 липня). Амоній хлор. Відновлено з cdc.gov.
- Університет Юти (2017). Таблетки з покриттям, що містять аммоний хлорид. RRecuperado dehealthcare.utah.edu.


