Гідроксид берилію (Be (OH) 2) хімічна структура, властивості та застосування
The гідроксид берилію являє собою хімічну сполуку, що складається з двох молекул гідроксиду (OH) і молекули берилію (Be). Його хімічна формула - Be (OH)2 і характеризується тим, що є амфотерним видом. Загалом, він може бути отриманий з реакції між монооксидом берилію і водою згідно з наступною хімічною реакцією: BeO + H2O → Be (OH)2
З іншого боку, це амфотерное речовина має молекулярну конфігурацію лінійного типу. Однак різні структури гідроксиду берилію можуть бути отримані: альфа-і бета-форма, як мінеральна і в паровій фазі, в залежності від використовуваного методу.
Індекс
- 1 Хімічна структура
- 1.1 Берилій гідроксид альфа
- 1.2 Бета-гідроксид берилію
- 1.3 Гідроксид берилію в мінералах
- 1.4 Парова гідроксид берилію
- 2 Властивості
- 2.1 Зовнішній вигляд
- 2.2 Термохімічні властивості
- 2.3 Розчинність
- 2.4 Ризики, викликані опроміненням
- 3 Використання
- 4 Отримання
- 4.1 Отримання металевого берилію
- 5 Посилання
Хімічна структура
Цей хімічний склад можна знайти чотирма різними способами:
Берилій гідроксид альфа
При додаванні будь-якого основного реагенту, такого як гідроксид натрію (NaOH) до розчину солі берилію, отримують альфа (α) форму гідроксиду берилію. Нижче наведено приклад:
2NaOH (розведений) + BeCl2 → Be (OH)22 + 2NaCl
2NaOH (розведений) + BeSO4 → Be (OH)2Na + Na2SO4
Берилій бета-гідроксид
Виродження цього альфа-продукту утворює метастабільну тетрагональну кристалічну структуру, яка після тривалого періоду часу була перетворена в ромбічну структуру під назвою берилієвий гідроксид бета (β)..
Ця бета-форма також отримують у вигляді осаду з розчину берилію натрію гідролізом в умовах, близьких до точки плавлення \ t.
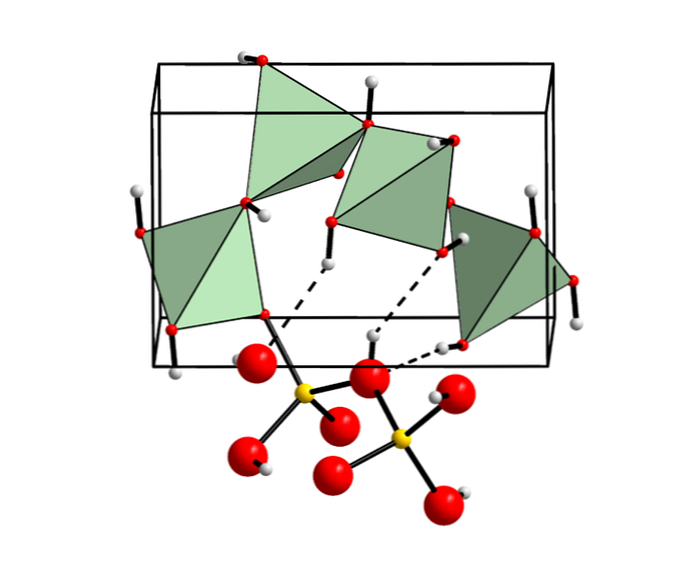
Гідроксид берилію в мінералах
Хоча це не є звичайним, гідроксид берилію виявляється як кристалічний мінерал, відомий як behoite (названий таким чином з посиланням на його хімічний склад).
Вона відбувається в гранітних пегматитах, що утворюються при зміні гадолініту (мінералів групи силікатів) у вулканічних фумаролах.
Цей відносно новий мінерал був вперше виявлений в 1964 році, і в даний час зустрічається тільки в гранітних пегматитах, розташованих у штатах Техас і Юта в США..
Пар гідроксиду берилію
При температурі вище 1200 ° C (2190 ° C) в паровій фазі існує гідроксид берилію. Виходить з реакції між водяною парою та берилієвим оксидом (BeO).
Аналогічно, отриманий пар має парціальний тиск 73 Па, виміряний при температурі 1500 ° С.
Властивості
Гідроксид берилію має молярну масу або приблизну молекулярну масу 43,0268 г / моль і щільність 1,92 г / см3. Його температура плавлення знаходиться при температурі 1000 ° C, в якій починається її розкладання.
Як мінерал, Be (OH)2 (behoita) має твердість 4, а щільність - від 1,91 г / см3 і 1,93 г / см3.
Зовнішній вигляд
Гідроксид берилію являє собою білу тверду речовину, яка у своїй альфа-формі має желатиновий і аморфний вигляд. З іншого боку, бета-форма цього з'єднання складається з чітко визначеної орторомбічної і стабільної кристалічної структури.
Можна сказати, що морфологія мінералу Be (OH)2 воно різноманітне, тому що його можна знайти як ретикулярні кристали, деревоподібні або сферичні агрегати. Аналогічно, він приходить у білий, рожевий, блакитний і навіть безбарвний і з жирним склоподібним блиском.
Термохімічні властивості
Ентальпія формування: -902,5 кДж / моль
Енергія Гіббса: -815,0 кДж / моль
Ентропія освіти: 45,5 Дж / моль
Теплоємність: 62,1 Дж / моль
Питома теплоємність: 1,443 Дж / К
Стандартна ентальпія освіти: -20,98 кДж / г
Розчинність
Гідроксид берилію за своєю природою є амфотерним, тому він здатний дарувати або приймати протони і розчиняє як кислотні, так і основні середовища в кислотно-основній реакції, виробляючи сіль і воду..
У цьому сенсі розчинність Be (OH)2 у воді обмежується розчинністю продукту Kps(H2O), яка дорівнює 6,92 × 10-22.
Ризики впливу
Нормативно допустима межа впливу на людину (PEL або OSHA) речовини гідроксиду берилію, визначена для максимальної концентрації між 0,002 мг / м3 і 0,005 мг / м3 становить 8 годин, а для концентрації 0,0225 мг / м3 максимум 30 хвилин.
Ці обмеження пов'язані з тим, що берилій класифікується як канцерогенний агент типу А1 (канцерогенний засіб у людей, виходячи з кількості доказів епідеміологічних досліджень)..
Використання
Використання гідроксиду берилію в якості сировини для переробки деякого продукту є дуже обмеженим (і незвичайним). Однак він є з'єднанням, що використовується в якості основного реагенту для синтезу інших сполук і отримання берилієвого металу.
Отримання
Оксид берилію (BeO) - хімічна сполука високої чистоти берилію, що найбільш часто використовується в промисловості. Характеризується як безбарвна тверда речовина з властивостями електричної ізоляції і високою теплопровідністю.
У цьому сенсі процес його синтезу (за технічною якістю) в первинному виробництві здійснюється наступним чином:
- Гідроксид берилію розчиняють у сірчаній кислоті (Н2SO4).
- Коли реакцію проводять, розчин фільтрують, так що нерозчинні домішки оксиду або сульфату усуваються таким чином..
- Фільтрат піддають випарюванню для концентрування продукту, який охолоджують з отриманням кристалів сульфату берилію BeSO.4.
- BeSO4 прожарюють при певній температурі між 1100 ° С і 1400 ° С.
Кінцевий продукт (BeO) використовується для виготовлення спеціальних керамічних виробів для промислового використання.
Отримання металевого берилію
Під час вилучення та переробки мінералів берилію утворюються домішки, такі як оксид берилію та гідроксид берилію. Останній піддають серії перетворень до отримання металевого берилію.
Be (OH) реагує2 розчином біфториду амонію:
Be (OH)2 + 2 (NH4) HF2 → (NH4)2BeF4 + 2 H2O
(NH4)2BeF4 він піддається підвищенню температури, що зазнає термічного розкладання:
(NH4)2BeF4 → 2NH3 + 2HF + BeF2
Нарешті, відновлення фториду берилію при температурі 1300 ° С з магнієм (Mg) призводить до отримання берилієвого металу:
BeF2 + Mg → Be + MgF2
Берилій використовується в металевих сплавах, виробництві електронних компонентів, виробництві радіаційних екранів і вікон, що використовуються в рентгенівському апараті.
Список літератури
- Вікіпедія. (s.f.). Гідроксид берилію. Отримано з en.wikipedia.org
- Holleman, A.F.; Wiberg, E. і Wiberg, N. (2001). Гідроксид берилію. Отримано з books.google.co.ve
- Publishing, M.D. (s.f.). Бехойте. Отримано з handbookofmineralogy.org
- Всі реакції. (s.f.). Берилій гідроксид Be (OH)2. Отримано з allreactions.com
- PubChem. (s.f.). Гідроксид берилію. Отримано з pubchem.ncbi.nlm.nih.gov
- Уолш, К. А. і Vidal, E.E. (2009). Хімія берилію та переробка. Отримано з books.google.co.ve


