Характерні аполярні молекули, як їх ідентифікувати і приклади
The аполярні молекули це ті, які в своїй структурі представляють симетричне розподіл їх електронів. Це можливо, якщо різниця електронегативності його атомів мала, або якщо електронегативні атоми або групи скасовують свої ефекти в молекулі.
Не завжди «аполярність» абсолютна. З цієї причини молекули полярної полярності іноді вважаються неполярними; тобто, він має диполярний момент, близький до 0. Тут входить рельєф місцевості відносно: наскільки низька повинна бути μ для молекули або сполуки, що вважається неполярною?
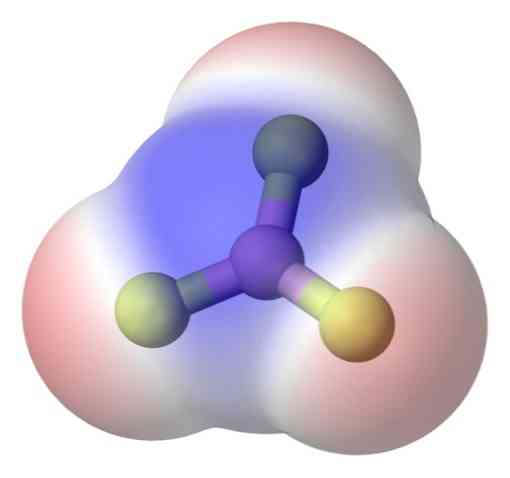
Для кращого вирішення проблеми у вас є молекула трифториду бору, BF3 (верхнє зображення).
Атом фтору набагато більш електронегативний, ніж атом бору, тому зв'язки B-F є полярними. Однак молекула BF3 є симетричною (тригональна площина) і передбачає векторну скасування трьох моментів B-F.
Таким чином, генеруються також аполярні молекули, навіть з існуванням полярних зв'язків. Сформована полярність може врівноважуватися існуванням іншої полярної ланки, такої ж величини, як і попередня, але орієнтованою в протилежному напрямку; як це відбувається в BF3.
Індекс
- 1 Характеристики аполярної молекули
- 1.1 Симетрія
- 1.2 Електронегативність
- 1.3 Міжмолекулярні сили
- 2 Як їх ідентифікувати?
- 3 Приклади
- 3.1 Благородні гази
- 3.2 Діатомічні молекули
- 3.3 Вуглеводні
- 3.4 Інше
- 4 Посилання
Характеристики аполярної молекули
Симетрія
Для того, щоб ефекти полярних зв'язків скасовували один одного, молекула повинна мати певну геометричну структуру; наприклад, лінійний, найлегший для розуміння на перший погляд.
Це стосується діоксиду вуглецю (CO2), яка має дві полярні ланки (O = C = O). Це пов'язано з тим, що два диполярних моменти зв'язків C = O скасовують один одного при зверненні до однієї сторони, а другий по відношенню до іншої, під кутом 180 °.
Тому одна з перших ознак, що враховується при оцінці «аполярності» молекули як пташиного ока, - це спостерігати, наскільки вона симетрична..
Припустимо, що замість CO2 у вас є молекула COS (O = C = S), яка називається сульфідом карбонілу.
Тепер це вже не аполярна молекула, оскільки електронегативність сірки менше, ніж у кисню; і, отже, дипольний момент C = S відрізняється від C = O. В результаті, COS - полярна молекула (як полярна мука з іншого мішка).
Нижнє зображення графічно підсумовує все, що тільки що було описано:
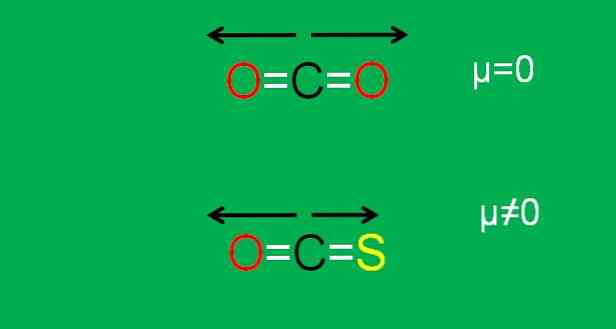
Зауважимо, що дипольний момент зв'язку C = S менше, ніж зв'язок C = O в молекулі COS.
Електронегативність
Електронегативність у шкалі Паулінга має значення між 0,65 (для францію) і 4,0 (для фтору). Загалом галогени мають високу електронегативність.
Коли різниця електронегативності елементів, які утворюють ковалентную зв'язок, менше або дорівнює 0,4, її називають аполярним або неполярним. Тим не менш, єдиними молекулами, які дійсно є неполярними, є ті, що утворюються зв'язками між ідентичними атомами (такими як водень, H-H)..
Міжмолекулярні сили
Для того, щоб речовина розчинялося у воді, воно повинно взаємодіяти з молекулами; взаємодій, які аполярні молекули не можуть зробити.
У аполярних молекулах їхні електричні заряди не обмежені в одному кінці молекули, а розподілені симетрично (або однорідно). Тому він не може взаємодіяти через диполь-дипольні сили.
Навпаки, аполярні молекули взаємодіють один з одним через дисперсійні сили Лондона; це миттєві диполи, які поляризують електронну хмару атомів сусідніх молекул. Тут молекулярна маса є переважним фактором фізичних властивостей цих молекул.
Як їх ідентифікувати?
-Можливо, одним з найкращих методів ідентифікації аполярної молекули є її розчинність в різних полярних розчинниках, які в цілому погано розчинні в них.
-Загалом, аполярні молекули мають газоподібний характер. Вони також можуть утворювати незмішувані рідини з водою.
-Неполярні тверді речовини характеризуються м'якістю.
-Сили дисперсії, які утримують їх разом, загалом слабкі. Через це їх точки плавлення або кипіння мають тенденцію бути нижчими, ніж температури сполук полярної природи.
-Неполярні молекули, особливо в рідкій формі, є поганими провідниками електрики, оскільки їм не вистачає чистого електричного заряду.
Приклади
Благородні гази
Хоча вони не є молекулами, благородні гази вважаються неполярними. Припускаючи, що протягом двох коротких періодів часу два його атоми взаємодіють, He-He, цю взаємодію можна вважати (наполовину) молекулою; молекули, які були б неполярними в природі.
Діатомічні молекули
Діатомічні молекули, такі як H2, Br2, я2, Cl2, O2, і F2, вони аполярні. Вони мають загальну формулу А2, A-A.
Вуглеводні
Що робити, якщо А - група атомів? Це було б до інших аполярних сполук; наприклад, етан, СН3-CH3, вуглецевий скелет лінійний, С-С.
Метан, СН4, і етан, C2H6, вони є аполярними молекулами. Вуглець має електронегативність 2,55; при цьому електронегативність водню дорівнює 2,2. Тому існує дипольний вектор низької інтенсивності, орієнтований від водню до вуглецю.
Але, внаслідок геометричної симетрії молекул метану і етану, сума дипольних векторів або дипольних моментів у їх молекулах дорівнює нулю, тому на молекулах немає чистого заряду..
Загалом те ж саме відбувається з усіма вуглеводнями, і навіть при наявності в них інсатурацій (подвійних і потрійних зв'язків) вони вважаються неполярними або малополярними сполуками. Аналогічно, циклічні вуглеводні являють собою аполярні молекули, такі як циклогексан або циклобутан..
Інші
Молекули діоксиду вуглецю (CO2) і сірковуглець (CS)2) є аполярними молекулами, як з лінійною геометрією.
У дисульфіду вуглецю електронегативність вуглецю становить 2,55, а електронегативність сірки - 2,58; так що обидва елементи мають, практично, однакову електронегативність. Не існує генерації дипольного вектора і, отже, чистий заряд дорівнює нулю.
Також ми маємо наступні молекули CCl4 і AlBr3, обидва аполярні:
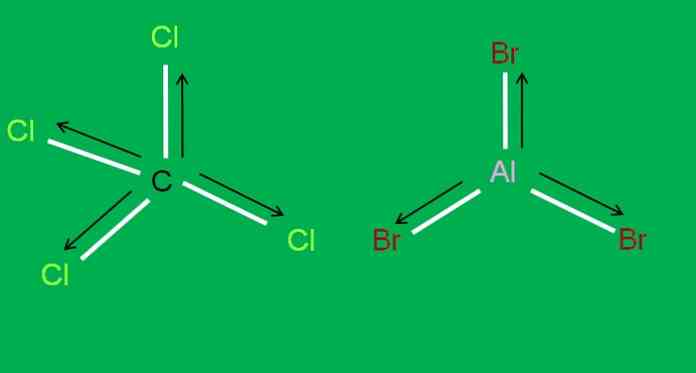
У трибромиде алюмінію, AlBr3 це відбувається так само, як з BF3, на початку статті. Між тим, для чотирихлористого вуглецю, CCl4, геометрія чотиригранна і симетрична, оскільки всі C-Cl ланки рівні.
Аналогічно, молекули з загальною формулою CX4 (CF4, CI4 і CBr4), вони також аполярні.
І, нарешті, аполярна молекула може навіть мати восьмигранну геометрію, як у випадку гексафториду сірки, SF6. Насправді, вона може мати будь-яку геометрію або структуру, якщо вона симетрична, а її електронний розподіл однорідний.
Список літератури
- Кері Ф. А. (2008). Органічна хімія Карбонові кислоти. (Шосте видання). Mc Graw Hill.
- Cedrón J., Landa V., Robles J. (2011). Полярність молекул. Отримано з: corinto.pucp.edu.pe
- Tutor Vista. (2018). Неполярна молекула. Отримано з: chemistry.tutorvista.com
- Helmenstine, Anne Marie, Ph.D. (28 січня 2019). Приклади полярних і неполярних молекул. Отримано з: thoughtco.com
- Куртус Р. (19 вересня 2016 р.). Полярні і неполярні молекули. Школа для чемпіонів. Отримано з: school-for-champions.com
- Ganong W. (2004). Медична фізіологія Видання 19го. Редакція сучасного керівництва.


