Сульфат алюмінію (Al2 (SO4) 3) структура, застосування, типи, токсичність
The сульфат алюмінію являє собою неорганічну сіль алюмінію формули Al2(SO4)3, що зазвичай з'являється у вигляді білого твердого тіла з блискучими кристалами. На колір з'єднання буде впливати його концентрація заліза і будь-яка інша домішка. Існує два основних типи сульфату алюмінію: А і В.
На нижньому зображенні показані білі кристали гідратованого сульфату алюмінію. Можна відзначити відсутність бурого забарвлення, що свідчить про іони заліза в кристалічній решітці.

Сульфат алюмінію - це сіль, яка дуже добре розчиняється у воді і в природі рідко зустрічається в його безводній формі. Він зазвичай гідратований у вигляді октадекагідрату сульфату алюмінію [Al2(SO4)3.18H2O] або гексадекагідрат [Al2(SO4)3.16H2O].
Крім того, він може утворювати подвійні солі з калієм, а також амоній, сполуки, відомі як квасцы. Частково це може бути пов'язано з спорідненістю води в гідратах для утримання інших іонів, крім алюмінію.
Сульфат алюмінію можна розкласти під дією води в гідроксиді алюмінію і сірчаної кислоти. Це властивість дозволило використовувати його як підкислювач ґрунтів.
Це також токсичне з'єднання, особливо при контакті з порошком. Однак вона має нескінченність застосувань і застосувань, які йдуть від очищення води за допомогою методу коагуляції, що відбувається через її використання в декількох галузях, до її використання з терапевтичними цілями..
Індекс
- 1 Структура
- 2 Що це (використовує)
- 2.1 Коагуляція або флокуляція води
- 2.2 Використання як протрава чорнила і в розробці паперу
- 2.3 Промислове використання
- 2.4 Лікарські та терапевтичні застосування
- 2.5 Інші види використання
- 3 Виробництво сульфату алюмінію
- 4 типи
- 5 Токсичність
- 6 Посилання
Структура
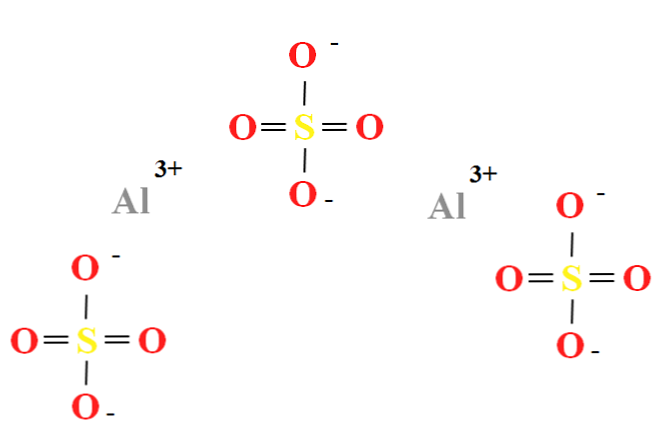
Сульфат алюмінію має співвідношення двох катіонів Al3+ для кожних трьох аніонів SO42- (верхнє зображення), яке можна спостерігати безпосередньо в його хімічній формулі Al2(SO4)3.
Зверніть увагу, що Al3+ вони сіруваті, тоді як SO42- вони жовті (для атома сірки) і червоні (для атомів кисню).
Ілюстрована структура відповідає безводній формі Al2(SO4)3, оскільки жодна молекула води не взаємодіє з іонами. Однак у ваших гідратах воду можна залучити до позитивних центрів Al3+, або негативними тетраедрами SO42- через водневі зв'язки (HOH-O-SO32-).
Al2(SO4)3H 18H2Або, наприклад, він містить 18 молекул води у своїй твердій структурі. Деякі з них можуть перебувати в безпосередньому контакті з Al3+ або з SO42-. Іншими словами: сульфат алюмінію може мати внутрішню або зовнішню координаційну воду.
Також в його структурі можуть бути розміщені інші катіони, такі як Fe3+, Na+, K+, і т.д. Але для цього необхідно наявність більше аніонів SO42-. Для чого? Для нейтралізації збільшення позитивних зарядів за рахунок металевих домішок.
Сульфат алюмінію може мати багато структур, хоча його гідрати прагнуть прийняти моноклінну кристалічну систему.
Фізико-хімічні властивості
Зовнішній вигляд
Він з'являється як тверда речовина з блискучими білими кристалами, гранулами або порошком.
Молекулярна маса
342,31 г / моль (безводний).
Запах
Це без запаху
Смак
Солодкий смак помірно в'яжучий.
Точка плавлення
Безводна форма 770º С (форма октадекадитрата 86,5º С)
Розчинність у воді
31,2 г / 100 мл при 0 ° С; 36,4 г / 100 мл при 20 ° С і 89 г / 100 мл при 100 ° С.
Щільність
2,67-2,71 г / см3.
Розчинність
Трохи розчиняється в етиловому спирті.
Тиск пари
По суті, нуль.
Стабільність
Стабільний у повітрі.
Розкладання
При нагріванні, приблизно при температурі його плавлення, він може розкладатися за рахунок виділення особливо оксиду сірки, токсичного газу.
Корозивність
Розчини сульфату алюмінію є корозійними для алюмінію. Також з'єднання може кородувати метали в присутності вологи.
pKa
3.3 - 3.6. А його рН становить 2,9 або більше в 5% -ному водному розчині.
Що це (використовує)
Коагуляція або флокуляція води
-При змішуванні з водою (питна, подана або відпрацьована), сульфат алюмінію викликає гідроксид алюмінію, який утворює комплекси з сполуками і частинки в розчині, що прискорює їх седиментацію, що за відсутності обробки сульфатом алюмінію буде приймати довгий час.
-Сульфат алюмінію також використовується при очищенні води басейну, що робить їх більш привабливими для використання.
-Завдяки використанню сульфату алюмінію вода отримується без помутніння і забарвлення, збільшуючи його питомість, полегшуючи очищення води. На жаль, цей спосіб очищення може призвести до дещо підвищеної концентрації алюмінію у воді.
-Алюміній - це дуже токсичний метал, який накопичується в шкірі, мозку і легенях, викликаючи серйозні розлади. Крім того, невідомо, яку функцію вона виконує в живих істотах.
-Європейський Союз вимагає, щоб максимальна дозволена межа алюмінію у воді не перевищувала 0,2 мг / л. Тим часом Агентство охорони навколишнього середовища США вимагає, щоб максимальна межа забруднення води алюмінієм не перевищувала 0,05-0,2 мг / л.
-Обробка стічних вод або використання з сульфатом алюмінію дозволяє усунути або зменшити фосфор в них, економічно.
Використовується як протрава чорнила і в розробці паперу
-Сульфат алюмінію використовується як протрава для барвників або фарб, допомагаючи закріпити на матеріалі, що підлягає фарбуванню. Його фіксуюча дія пов'язана з Al (OH)3, чия желатинова консистенція сприяє адсорбції барвників на текстилі.
-Незважаючи на те, що з 2000 року до н.е. для описаної мети вона застосовувалася, тільки органічні барвники вимагають протравлення. Синтетичні барвники, з іншого боку, не вимагають стирання для виконання своєї функції.
-Вона була витіснена з виробництва паперу, але вона все ще використовується у виробництві паперової маси. Видаляє домішки, а також використовується для зв'язування матеріалів, нейтралізує заряд і калібрує каніфоль.
Промислове використання
-Використовується в будівельній індустрії з метою прискорення налаштування бетону. Крім того, він використовується в гідроізоляції будівель.
-У промисловості мила і жирів вона використовується у виробництві гліцерину.
-Застосовується в нафтовій промисловості при виготовленні синтетичних каталізаторів, які використовуються під час експлуатації.
-Застосовується в фармацевтичній промисловості як в'яжучий засіб при приготуванні препаратів і косметичних засобів.
-Втручається у виробництво барвників, таких як кармін. Він також використовується як барвник у виробництві синтетичних каучуків бутадієнстиролу.
-У цукровій промисловості використовується як очищувач меляси для цукрової тростини.
-Застосовується при виготовленні дезодорантів. Чому? Тому що він викликає звуження протоки потових залоз, що обмежує накопичення поту, необхідного середовища для росту бактерій, що викликають запах..
-Застосовується в дубленні шкіри, необхідний процес для його використання. Крім того, він використовується у виробництві добрив.
-Використовується в якості добавки при приготуванні фарб, клеїв і герметиків, а також для чищення та догляду за меблями..
Лікарські та терапевтичні застосування
-Сульфат алюмінію є імунологічним допоміжним засобом. Таким чином, він виконує функцію обробки антигенів таким чином, що, вивільняючись на їхньому місці дії, вони продукують більшу продукцію антитіл для антигенів, які були щеплені.
-Ад'ювант Фрейнда і БЦЖ, а також інші ад'юванти, включаючи ендогенні, такі як інтерлейкіни, неспецифічні для антигенів, що дозволяє збільшити радіус імунної дії. Це дозволило розробити вакцини проти численних захворювань.
-Коагулююча дія сульфату алюмінію дозволила усунути численні віруси в обробленій воді, серед інших: Q бета, MS2, T4 і P1. Результати вказують на те, що обробка води сульфатом алюмінію призводить до інактивації таких вірусів.
-Сульфат алюмінію застосовується у вигляді палички або порошку для лікування невеликих поверхневих ран або подряпин, що виникають при голінні.
-Він використовується при виробництві ацетату алюмінію, з'єднання, що використовується при лікуванні деяких умов вуха. Він також використовувався, без значного успіху, для полегшення наслідків пожежогасіння..
-Розчини сульфату алюмінію використовують у концентрації від 5% до 10% для місцевого лікування виразок, що дозволяють контролювати їх виділення.
-В'яжуча дія сульфату алюмінію стискає поверхневі шари шкіри, коагулюючи білки і загоюючи рани.
Інші види використання
-Сульфат алюмінію допомагає контролювати надмірний ріст водоростей у ставках, озерах і потоках води. Вона також використовується при видаленні молюсків, серед інших іспанських слимаків.
-Садівники застосовують цю суміш для підкислення лужних ґрунтів. При контакті з водою сульфат алюмінію розкладають на гідроксид алюмінію і розбавляють сірчану кислоту. Потім осаджується гідроксид алюмінію, залишаючи сірчану кислоту в розчині.
-Підкислення ґрунтів за рахунок сірчаної кислоти візуалізується дуже творчо, внаслідок існування рослини під назвою «гортензія», квіти якої синіють у присутності кислого ґрунту; тобто вони чутливі і реагують на зміни рН.
-Сульфат алюмінію бере участь у виробництві піни для боротьби і контролю вогню. Як? Реагує з бікарбонатом натрію, виробляючи вивільнення CO2. Це газові блоки O доступу2 до місця згоряння матеріалу; і, отже, припинення вогню, яке розвивалося.
Виробництво сульфату алюмінію
Сульфат алюмінію синтезують шляхом взаємодії збагаченого алюмінієм з'єднання, такого як бокситова руда, з сірчаною кислотою при підвищених температурах. Наступне хімічне рівняння являє собою реакцію:
Al2O3 + H2SO4 -> Al2(SO4)3 + 3 H2O
Сульфат алюмінію також може бути утворений реакцією нейтралізації між гідроксидом алюмінію і сірчаною кислотою згідно з наступною реакцією:
2 Al (OH)3 + 3 H2SO4 + 12 H2O -> Al2(SO4)3.18H2O
Сірчана кислота реагує з алюмінієм з утворенням сульфату амонію і вивільненням молекул водню у вигляді газу. Реакція схематизується наступним чином:
2 Al + 3 H2SO4 -> Al2(SO4)3 + 3 H2
Типи
Сульфат алюмінію класифікується на два типи: тип А і тип В. В сульфаті алюмінію типу А тверді речовини є білими і мають концентрацію заліза менше 0,5%.
У сульфаті алюмінію типу В тверді речовини бурі і мають концентрацію заліза менше 1,5%.
Є галузі, що виробляють сульфат алюмінію, які мають різні критерії їх класифікації. Таким чином, галузь повідомляє про її приготування сульфату алюмінію типу А максимальною концентрацією 0,1% заліза як оксиду заліза. Хоча для типу B вони вказують максимальну концентрацію заліза 0,35%.
Токсичність
-Сульфат алюмінію - це з'єднання, яке проявляє свою токсичну дію при контакті з пилом, викликаючи при цьому подразнення шкіри, а в тих випадках, коли часто зустрічається, дерматит.
-У очах це викликає сильне роздратування, навіть для отримання постійних травм.
-Вдихання викликає роздратування носа і горла, що може викликати кашель і висипання.
-Його споживання викликає подразнення шлунка, нудоту і блювоту.
-Є токсичні ефекти, які, хоча вони безпосередньо не пов'язані з сульфатом алюмінію, вони опосередковано обумовлені їх використанням. Це випадок певних токсичних ефектів алюмінію, викликаних використанням сульфату алюмінію при очищенні води.
-Пацієнти, які хронічно діалізуються з використанням солей, приготовлених у очищеній воді, за допомогою використання сульфату алюмінію, відчувають дуже важкі порушення здоров'я. Серед цих розладів ми маємо анемію, деменцію шляхом діалізу і збільшення захворювань кісток.
Список літератури
- Вікіпедія. (2018). Сульфат алюмінію Взяті з сайту: en.wikipedia.org
- Aris Industrial Розчин сульфату алюмінію типу А і В. Взяті з: aris.com.pe
- Крістофер Бойд (9 червня 2014 року). Топ промислового використання для сульфату алюмінію. Взяті з: chemservice.com
- PubChem. (2018). Сульфат алюмінію безводний. Взяті з: pubchem.ncbi.nlm.nih.gov
- Andesia Chemicals (20 серпня 2009 року). Запобіжний лист сульфату алюмінію. [PDF] Взяті з: andesia.com
- Хімічна книга. (2017). Сульфат алюмінію. Взяті з: chemicalbook.com


