Хімічна структура, властивості та застосування сульфату амонію
The сульфат амонію Він являє собою потрійну і аміачну неорганічну сіль сірчаної кислоти. Його хімічна формула (NH4)2SO4. Отже, стехіометричні пропорції говорять, що для кожного аніона сульфату є два катіона амонію, що взаємодіють з ним. Це дозволяє нейтральність солі ((+1) ∙ 2 + (-2)).
Його номенклатура обумовлена тим, що вона являє собою сіль, отриману з Н2SO4, змінюючи суфікс "урік" на "ато". Таким чином, два початкових протони замінені на NH4+, продукт реакції з аміаком (NH3). Тоді хімічне рівняння для його синтезу становить: 2 NH3 + H2SO4 => (NH4)2SO4
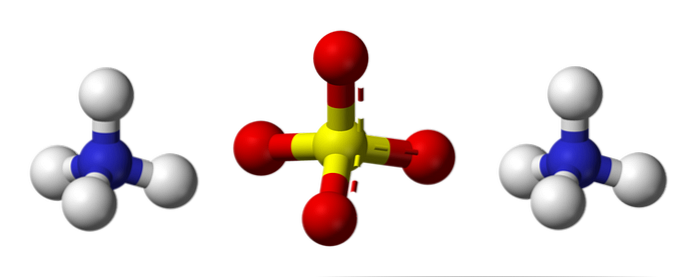
Сульфат амонію є сховищем азоту і сірки, як незамінний в хімії грунтів і добрив.
Індекс
- 1 Хімічна структура
- 2 Фізико-хімічні властивості
- 2.1 Молекулярна маса
- 2.2 Фізичний вигляд
- 2.3 Запах
- 2.4 Точка плавлення
- 2.5 Розчинність
- 2.6 Щільність
- 2.7 Тиск пари
- 2.8 Точка спалаху
- 2,9 рН
- 2.10 Стабільність
- 2.11 Розкладання
- 2.12 Корозія
- 3 Використання
- 3.1 У сільському господарстві
- 3.2 Як аналітичний реагент
- 3.3 При осадженні та виділенні білків
- 3.4 У галузі
- 3.5 Інші види використання
- 4 Посилання
Хімічна структура
Верхнє зображення ілюструє молекулярні геометрії іонів NH4+ і SO42-. Червоним сферам відповідають атоми кисню, білі сфери відповідають атомам водню, сині сфери атому азоту і жовті сфери відповідають атому сірки..
Обидва іона можна розглядати як два тетраедра, що володіє трьома одиницями, які взаємодіють, утворюючи орторомбічну структуру кристалів. Сульфат-аніон являє собою SO42- і здатний пожертвувати або приймати чотири водневі зв'язки, як і катіон NH4+.
Фізико-хімічні властивості
Молекулярна маса
132,134 г / моль.
Зовнішній вигляд
Суцільний білий. Орторомбічні білі або коричневі кристали в залежності від домішкових рівнів.
Запах
Туалет.
Точка плавлення
280 ºC. Ця температура плавлення, низька порівняно з іншими іонними сполуками, обумовлена тим, що вона являє собою сіль з одновалентними катіонами (+1) і з різними іонами за своїми розмірами, змушуючи тверде тіло мати низьку кристалічну ретикулярну енергію..
Розчинність
76,4 г / 100 г води при 25 ° С. Ця спорідненість до води обумовлена великою здатністю її молекул до сольвації іонів амонію. З іншого боку, він нерозчинний в ацетоні і в спирті; тобто в розчинниках, менш полярних, ніж вода.
Щільність
1,77 г / см3 при 25 ºC.
Тиск пари
1,871 кПа при 20 ºC.
Точка горючості
26 ºC.
рН
5,0-6,0 (25 ° С, 1 М розчин). Незначно кислий рН обумовлений гідролізом NH4+ у воді, що продукує Н3O+ при низьких концентраціях.
Стабільність
Стабільний у відповідних умовах навколишнього середовища. При контакті з сильними окислювачами може загорятися.
Розкладання
Він починає розкладатися при 150 ºC, вивільняючи токсичні пари оксиду сірки, оксиду азоту та амонію.
Корозія
Не атакує залізо або алюміній.
Використання

У сільському господарстві
- Сульфат амонію використовується як добриво в лужних грунтах. Амонієва сіль має 21% азоту і 24% сірки у своєму складі. Однак є сполуки, які забезпечують більшу кількість азоту, ніж сульфат амонію; Перевагою останньої є висока концентрація сірки.
- Сірка має важливе значення в синтезі білків, оскільки кілька амінокислот - такі як цистин, метіонін і цистеїн - мають сірку. З цих причин сульфат амонію залишається одним з найважливіших добрив.
- Використовується в посівах пшениці, кукурудзи, рису, бавовни, картоплі, конопель і плодових дерев.
- Низький рН лужних грунтів обумовлений їх вкладом у процес нітрифікації, що здійснюється мікробами. Використовують амоній (NH)4+) для отримання нітрату (NO3-) і вивільняють H+: 2NH4+ + 4O2 => 2NO3- + 2H2O + 4H+. Збільшення концентрації водню знижує рН лужних ґрунтів і дозволяє більше використовувати.
- На додаток до використання в якості добрива, сульфат амонію виступає як коад'ювант для розчинних інсектицидів, гербіцидів та фунгіцидів, які розпилюються на культури..
- Сульфат здатний виділяти іони, присутні в ґрунті і в зрошувальній воді, які необхідні для життя певних патогенів. Серед іонів, які захоплюють сульфат амонію, є Ca2+, Mg2+, Віра2+ і Віра3+. Ця дія посилює мікробіцидну дію зазначених агентів.
В якості аналітичного реагенту
Сульфат амонію виступає в якості осаждающего агента в електрохімічному аналізі, в мікробіологічних культуральних середовищах і в приготуванні солей амонію.
При осадженні і виділенні білків
Сульфат амонію використовується при виділенні та очищенні білків, особливо білків плазми. Кількість сульфату амонію додається до плазми до певної концентрації; таким чином, викликається осадження групи білків.
Осад збирають центрифугуванням і до супернатанту додають додаткову кількість сульфату амонію і при новій концентрації відбувається осадження іншої групи білків..
Повторення попереднього процесу в послідовній формі дозволяє отримати в результаті різні фракції білків плазми.
Перед появою нових технологій молекулярної біології ця процедура дозволила виділити білки плазми, що мають велике значення в медицині, наприклад, імуноглобуліни, фактори згортання крові та ін..
У промисловості
Сульфат амонію впливає на гальмування початку пожежі в текстильній промисловості. Використовується як добавка в гальванічній промисловості. Використовується також у виробництві перекису водню, хлориду амонію тощо..
Інші види використання
- Сульфат амонію використовують в якості регулюючого агента осмотичного тиску і в якості засобу для осадження солі.
- У вигляді лаурилсульфату амонію поверхневий натяг води зменшується, що дозволяє розділяти забруднюючі речовини за рахунок збільшення твердості води.
- Це антикорозійний засіб.
- Застосовується як харчова добавка, що регулює кислотність у борошні та хлібі.
Список літератури
- ОЕСР СІДС. (Жовтень 2004 року). Сульфат амонію. [PDF] Отримано 27 квітня 2018 року від: inchem.org
- Мозаїчна компанія. (2018). Сульфат амонію. Отримано 27 квітня 2018 року з: cropnutrition.com
- Вікіпедія. (2018). Сульфат амонію. Отримано 27 квітня 2018 року з: en.wikipedia.org
- Pubchem. (2018). Сульфат амонію. Отримано 27 квітня 2018 року з: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23 липня 2015 р.) [Малюнок] Отримано 27 квітня 2018 року з: flickr.com
- Паула Папп (22 лютого 2017 року). Застосування і застосування сульфату амонію. Отримано 27 квітня 2018 року з: business.com


