Структура, властивості, номенклатура та застосування оксиду срібла (Ag2O)
The оксид срібла являє собою неорганічне з'єднання, хімічна формула якого є Ag2О. Сила, що об'єднує його атоми, має цілком іонну природу; тому вона складається з іонного твердого тіла, де є співвідношення двох катіонів+ взаємодіє електростатично з аніоном O2-.
Аніон оксиду, O2-, це є результатом взаємодії атомів срібла поверхні з киснем середовища; дуже схожим чином на залізо і багато інших металів. Шматок срібла або прикраси замість почервоніння і руйнування в іржі стає чорним, властивим оксиду срібла.

Наприклад, на зображенні вище можна побачити іржаву срібну чашку. Зверніть увагу на її потемнілу поверхню, хоча вона все ще зберігає деякий декоративний блиск; Тому навіть іржаві предмети срібла можна вважати досить привабливими для декоративного використання.
Властивості оксиду срібла такі, що вони не псують, на перший погляд, вихідну металеву поверхню. Утворюється при кімнатній температурі шляхом простого контакту з киснем повітря; і ще цікавіше, він може розкладатися при високих температурах (вище 200 ° C).
Це означає, що якщо скло зображення було утримано, і тепло інтенсивного полум'я було застосовано, воно відновило б свій сріблястий блиск. Тому його формування є термодинамічно оборотним процесом.
Оксид срібла також має інші властивості і, поза його простою формулою Ag2Або вона охоплює складні структурні організації та багату різноманітність твердих тіл. Однак Ag2Або це, можливо, поруч з Ag2O3, найбільш представницький з оксидів срібла.
Індекс
- 1 Структура оксиду срібла
- 1.1 Зміни з числом Валенсії
- 2 Фізико-хімічні властивості
- 2.1 Молекулярна маса
- 2.2 Зовнішній вигляд
- 2.3 Щільність
- 2.4 Точка плавлення
- 2,5 Кп
- 2.6 Розчинність
- 2.7 Ковалентний характер
- 2.8 Розкладання
- 3 Номенклатура
- 3.1 Valencias I і III
- 3.2 Систематична номенклатура складних оксидів срібла
- 4 Використання
- 5 Посилання
Структура оксиду срібла
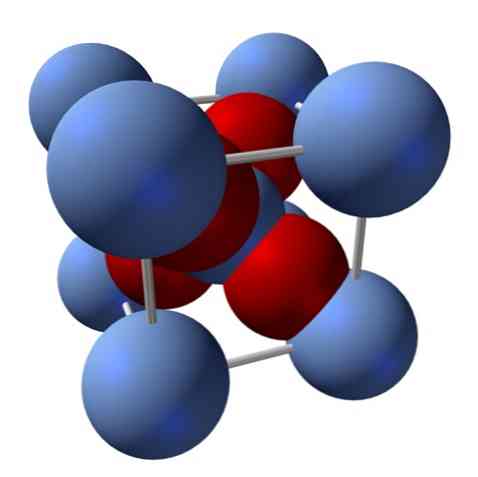
Якою є її структура? Як згадувалося на початку: це іонна тверда речовина. З цієї причини не може бути ковалентних зв'язків Ag - O і Ag = O в його структурі; оскільки, якщо б вони були, властивості цього оксиду різко змінилися. Це тоді іони Ag+ і O2- у співвідношенні 2: 1 і відчувають електростатичне притягання.
Структура оксиду срібла визначається внаслідок того, яким чином іонні сили розташовуються в просторі іонами Ag+ і O2-.
У верхньому зображенні, наприклад, є одинична комірка для кубічної кристалічної системи: катіони Ag+ є срібні блакитні сфери і О2- червонуваті сфери.
Якщо підрахувати кількість сфер, ви побачите, що на перший погляд є дев'ять сріблясто-синіх і чотирьох червоних кольорів. Однак враховуються тільки фрагменти сфер, що містяться в кубі; для підрахунку цих часток, які є частками сумарних сфер, необхідно виконати співвідношення 2: 1 для Ag2O.
Повторення структурної одиниці тетраедра AgO4 оточений ще чотирма Аг+, побудовано все чорне тверде тіло (усунення проміжків або нерівностей, які можуть мати ці кристалічні домовленості).
Змінюється з числом Валенсія
Орієнтуючись тепер не на тетраедр AgO4 але в лінії АгоАг (спостерігати вершини верхнього куба), тверде тіло оксиду срібла складається, з іншої точки зору, з декількох іонних шарів, розташованих лінійно (хоча й похило). Все це в результаті "молекулярної" геометрії навколо Ag+.
Зазначене підтверджено кількома дослідженнями його іонної структури.
Срібло працює переважно з валентністю +1, оскільки при втраті електрона отримана електронна конфігурація [Kr] 4d10, що є дуже стабільним. Інші валентності, такі як Ag2+ і Ag3+ вони менш стійкі, оскільки втрачають електрони з орбіталей майже повністю заповнені.
Іон Ag3+, однак воно порівняно менш нестійке порівняно з Ag2+. Фактично, вона може співіснувати в компанії Ag+ Хімічно збагачує структуру.
Його електронна конфігурація [Kr] 4d8, з непарними електронами таким чином, що дає їй певну стабільність.
На відміну від лінійної геометрії навколо іонів Аг+, встановлено, що іонів Ag3+ Це квадратна квартира. Тому оксид срібла з іонами Ag3+ складається з шарів, що складаються з квадратів AgO4 (не тетраедрів) електростатично пов'язаних лініями AgOAg; Такий випадок Ag4O4 Ag2O. Ag2O3 з моноклінною структурою.
Фізико-хімічні властивості

Якщо подряпати поверхню срібної чашки головного зображення, ви отримаєте тверде тіло, яке не тільки чорне, але також має коричневі або коричневі тони (верхнє зображення). Деякі з його фізичних і хімічних властивостей, про які повідомляють моменти, є такими:
Молекулярна маса
231,735 г / моль
Зовнішній вигляд
Тверда чорна коричнева у вигляді порошку (зауважте, що незважаючи на те, що вона є іонним твердим речовиною, вона не має кристалічного вигляду). Він без запаху і змішаний з водою надає йому металевий смак
Щільність
7,14 г / мл.
Точка плавлення
277-300 ° С. Звичайно, він тане в тверде срібло; тобто він, ймовірно, розпадається перед утворенням рідкого оксиду.
Кп
1.52. 10-8 у воді при 20 ° С. Отже, він є сполукою, що мало розчиняється у воді.
Розчинність
Якщо уважно поглянути на образ її структури, ви побачите, що сфери Ag2+ і O2- Вони не розходяться майже в розмірах. В результаті тільки маленькі молекули можуть проникати всередину кристалічної решітки, роблячи її нерозчинною майже у всіх розчинниках; за винятком тих, де він реагує, таких як основи і кислоти.
Ковалентний характер
Хоча неодноразово було сказано, що оксид срібла є іонним з'єднанням, деякі властивості, такі як його низька температура плавлення, суперечать цьому твердженню..
Звичайно, розгляд ковалентного характеру не руйнує те, що пояснюється його структурою, достатньо було б додати його до структури Ag \ t2Або модель сфер і стержнів для позначення ковалентних зв'язків.
Також, тетраедри і квадратні площини AgO4, як і лінії AgOAg, вони будуть пов'язані ковалентними (або ковалентними іонними) зв'язками.
Маючи це на увазі, Ag2Або це буде фактично полімер. Проте рекомендується розглядати його як іонне тверде тіло з ковалентним характером (чия природа цього зв`язку все ще залишається проблемою на сьогоднішній день).
Розкладання
Спочатку було зазначено, що його формування є термодинамічно оборотним, тому він поглинає тепло, щоб повернутися до свого металевого стану. Все це можна виразити двома хімічними рівняннями для таких реакцій:
4Ag (s) + O2(g) => 2Ag2O (s) + Q
2Ag2O (s) + Q => 4Ag (s) + O2(g)
Де Q являє тепло в рівнянні. Це пояснює, чому вогонь, що спалює поверхню іржавої срібної чашки, повертає його сріблястий блиск.
Тому важко припустити, що існує Ag2O (l), оскільки миттєво розкладаються теплом; якщо, тиск є занадто високим для отримання зазначеної коричневої чорної рідини.
Номенклатура
При можливості введення іонів Ag2+ і Ag3+ крім загальної і переважаючої Ag+, термін "оксид срібла" починає здаватися недостатнім для позначення Ag2O.
Це пояснюється тим, що іон Ag+ більше рясніше, ніж інші, так що Аг береться2Або як єдиний оксид; що взагалі не є правильним.
Якщо ви вважаєте Ag2+ як практично неіснуючої з урахуванням її нестабільності, тоді будуть присутні тільки іони з валентностями +1 і +3; тобто Ag (I) і Ag (III).
Валенсія I і III
Будучи найменшою валентністю Ag (I), її називають додаванням суфікса -oso до його назви argentum. Отже, Ag2Або він: аргентозооксид або, за систематичною номенклатурою, дипломат монооксид.
Якщо Ag (III) повністю ігнорується, то його традиційна номенклатура повинна бути: оксид срібла замість оксиду аргентини.
З іншого боку, Ag (III), що є більшою валентністю, додає суфікс -ico до його назви. Отже, Ag2O3 є: оксид срібла (іони 2 Ag)3+ з трьома O2-). Крім того, його назва за систематичною номенклатурою буде: дипломат триоксид.
Якщо спостерігається структура Ag2O3, можна припустити, що він є продуктом окислення озоном, OR3, замість кисню. Тому його ковалентний характер повинен бути більшим, оскільки він є ковалентним з'єднанням з зв'язками Ag-O-O-Ag або Ag-O.3-Ag.
Систематична номенклатура складних оксидів срібла
AgO, також написаний як Ag4O4 Ag2O. Ag2O3, це оксид срібла (I, III), оскільки має як валентності +1, так і +3. Його назва за систематичною номенклатурою буде наступним: тетраатрид тетраоксид.
Ця номенклатура дуже допомагає, коли йдеться про інші стехіометрично більш складні оксиди срібла. Наприклад, припустимо два твердих речовини 2Ag2O. Ag2O3 і Ag2O A 3Ag2O3.
Написання першого у більш підходящий спосіб буде: Ag6O5 (підрахунок і додавання атомів Ag і O). Його ім'я буде потім гексаплатовим пентоксидом. Зауважимо, що цей оксид має композицію срібла, меншу, ніж Ag2O (6: 5) < 2:1).
При написанні другого твердого тіла в іншому випадку це буде: Ag8O10. Його назва буде octaplate decaoxide (з 8:10 або 4: 5 співвідношення). Цей гіпотетичний оксид срібла був би "дуже окислений".
Використання
Досі проводяться дослідження в пошуках нових і складних видів використання оксиду срібла. Деякі з його застосувань перелічені нижче:
-Він розчиняється в аміаку, аміачної селітри та воді з утворенням реагенту Tollens. Цей реагент є корисним інструментом у якісному аналізі в лабораторіях органічної хімії. Це дозволяє визначити наявність альдегідів у зразку, позитивна відповідь - формування «срібного дзеркала» в пробірці.
-Разом з металевим цинком він утворює первинні батареї срібла оксиду цинку. Це, мабуть, одне з найпоширеніших і найпоширеніших способів його використання.
-Він служить в якості газоочистителя, поглинаючи, наприклад, CO2. При нагріванні він випускає захоплені гази і може бути повторно використаний кілька разів.
-Завдяки антимікробним властивостям срібла, його оксид корисний в дослідженнях біоаналізу та очищення ґрунту.
-Це м'який окислювач, здатний окислювати альдегіди до карбонових кислот. Він також використовується в реакції Хофмана (третинні аміни) і бере участь в інших органічних реакціях, як реагент або каталізатор.
Список літератури
- Bergstresser M. (2018). Оксид срібла: Формула, розкладання і утворення. Дослідження. Отримано з: study.com
- Автори та редактори обсягів III / 17E-17F-41C. (s.f.). Срібні оксиди (Ag (x) O (y)) кристалічна структура, параметри решітки. (Чисельні дані і функціональні відносини в науці і техніці), том 41С. Спрінгер, Берлін, Гейдельберг.
- Махендра Кумар Тріведі, Рама Мохан Таллапраграда, Еліс Брантон, Дахрін Тріведі, Гопал Наяк, Омпракаш Латіал, Снехасіс Яна. (2015). Потенційний вплив біоенергетичного лікування на фізичні та теплові властивості порошку оксиду срібла. Міжнародний журнал біомедичної науки і техніки. Том 3, № 5, с. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Салліван Р. (2012). Розкладання оксиду срібла. Університет Орегона Отримано з: chemdemos.uoregon.edu
- Флінт, Дейянда. (24 квітня 2014 р.) Використання батарей срібного оксиду. Наука. Отримано з: sciencing.com
- Салман Монтасір Е. (2016). Дослідження деяких оптичних властивостей оксиду срібла (Ag2o) з використанням UVVisable спектрофотометра. [PDF] Отримано з: iosrjournals.org
- Bard Allen J. (1985). Стандартний потенціал у водному розчині. Марсель Деккер. Отримано з: books.google.co.ve


