Структура, властивості, номенклатура та застосування оксиду золота (III) (Au2O3)
The оксид золота (III) являє собою неорганічне з'єднання, хімічна формула якого є Au2O3. Теоретично можна очікувати, що її природа буде ковалентним типом. Однак наявність певного іонного характеру в його твердому тілі взагалі не може бути відкинуто; або те ж саме, припускають відсутність катіона3+ поряд з аніоном O2-.
Може здатися суперечливим, що золото, будучи благородним металом, може іржавіти. За нормальних умов шматочки золота (як і зірки на зображенні нижче) не можуть бути окислені при контакті з киснем в атмосфері; однак при опроміненні ультрафіолетовим випромінюванням в присутності озону, OR3, малюнок інший.

Якби золоті зірки піддавалися цим умовам, вони стали б червонувато-коричневими, характерними для Au2O3.
Інші способи отримання цього оксиду включають хімічну обробку зазначених зірок; наприклад, перетворення маси золота у відповідний хлорид AuCl3.
Після, до AuCl3, і утворилися інші можливі солі золота, додають сильну основну середу; і при цьому отримують гідратований оксид або гідроксид, Au (OH)3. Нарешті, останнє з'єднання термічно зневоднюють для отримання Au2O3.
Індекс
- 1 Структура оксиду золота (III)
- 1.1 Електронні аспекти
- 1.2
- 2 Властивості
- 2.1 Фізичний вигляд
- 2.2 Молекулярна маса
- 2.3 Щільність
- 2.4 Точка плавлення
- 2.5 Стабільність
- 2.6 Розчинність
- 3 Номенклатура
- 4 Використання
- 4.1 Забарвлення окулярів
- 4.2 Синтез ауратов і вибухаючого золота
- 4.3 Обробка самоскладених моношарів
- 5 Посилання
Структура оксиду золота (III)
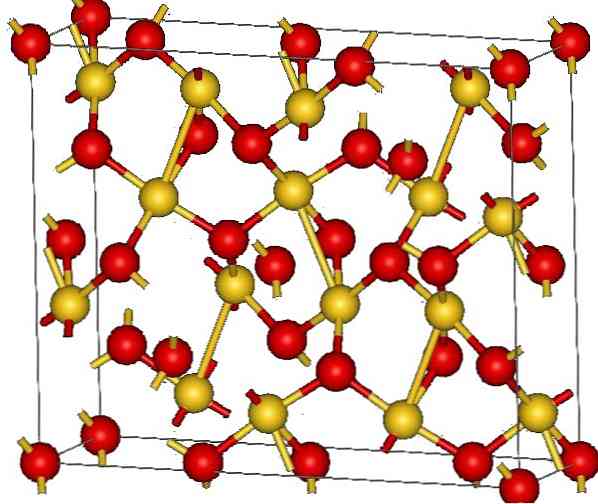
На верхньому зображенні показана кристалічна структура оксиду золота (III). Показано розташування атомів золота і кисню в твердому тілі, або як нейтральні атоми (ковалентне тверде тіло), або як іони (іонне тверде речовина). Неясно, що в будь-якому випадку достатньо усунути або помістити посилання Au-O.
Відповідно до зображення, передбачається, що ковалентний символ переважає (що було б логічним). З цієї причини представлені атоми та зв'язки показані відповідно зі сферами та гратами. Золоті сфери відповідають атомам золота (AuIII-O), і червонуваті до атомів кисню.
Якщо ви уважно подивитеся, ви побачите, що є одиниці AuO4, які з'єднуються атомами кисню. Іншим способом візуалізації було б врахувати, що кожен Au3+ оточений чотирма O2-; Звичайно, з іонної точки зору.
Ця структура є кристалічною, тому що атоми впорядковуються, підпорядковуючись тій же дальній картині. Таким чином, його унітарна клітина відповідає ромбоедричній кристалічній системі (так само, як у верхньому зображенні). Тому всі Au2O3 можна було б побудувати, якби всі ті сфери елементарної комірки були розподілені в просторі.
Електронні аспекти
Золото є перехідним металом, і можна очікувати, що його 5d-орбіталі безпосередньо взаємодіють з 2p-орбіталями атома кисню. Таке перекриття їх орбіталей теоретично повинно генерувати смуги провідності, які перетворюють Au2O3 у твердому напівпровіднику.
Тому справжню структуру Au2O3 це ще складніше з цим.
Гідрати
Золотий оксид може утримувати молекули води в межах своїх ромбоедричних кристалів, що призводить до появи гідратів. Коли такі гідрати утворюються, структура стає аморфною, тобто невпорядкованою.
Хімічна формула таких гідратів може бути будь-якою з наступних, яка насправді не є глибоко прояснена: Au2O3. ZH2O (z = 1, 2, 3 і т.д.), Au (OH)3, або AuxOі(OH)z.
Формула Au (OH)3 являє собою спрощення справжньої композиції зазначених гідратів. Це пояснюється тим, що в межах гідроксиду золота (III) дослідники також виявили наявність Au2O3; і, отже, має сенс обробляти його в ізоляції як "простий" гідроксид перехідного металу.
З іншого боку, тверда речовина з формулою AuxOі(OH)z можна очікувати аморфної структури; оскільки, це залежить від коефіцієнтів x, і і z, чиї зміни призвели до виникнення всіх видів структур, які навряд чи могли б мати кристалічну картину.
Властивості
Зовнішній вигляд
Це тверда речовина червонувато-коричневого кольору.
Молекулярна маса
441,93 г / моль.
Щільність
11,34 г / мл.
Точка плавлення
Плавиться і розкладається при 160ºC. Тому не вистачає температури кипіння, тому цей оксид ніколи не досягає точки кипіння.
Стабільність
Au2O3 вона термодинамічно нестабільна, оскільки, як згадувалося на початку, золото не має тенденції окислюватися при нормальних температурних умовах. Так легко зводиться, щоб знову стати благородним золотом.
Чим вище температура, тим швидше реакція, яка відома як термічне розкладання. Отже, Au2O3 при 160 ° С він розкладається для отримання металевого золота і вивільнення молекулярного кисню:
2 Au2O3 => 4 Au + 3 O2
Дуже подібна реакція може відбуватися з іншими сполуками, що сприяють зменшенню. Чому зменшення? Тому що золото повертається, щоб отримати електрони, які кисень забрав з нього; це те ж саме, що кажуть, що вона втрачає зв'язок з киснем.
Розчинність
Це тверда речовина, нерозчинна у воді. Однак він розчинний у соляній кислоті і азотній кислоті, внаслідок утворення хлоридів золота і нітратів.
Номенклатура
Золотий оксид (III) - назва, що регулюється номенклатурою запасів. Інші способи згадати це:
-Традиційна номенклатура: оксид аурерика, тому що валентність 3+ є найвищою для золота.
-Систематична номенклатура: діорокіс.
Використання
Забарвлення окулярів
Одним з найвідоміших його використання є надання червоних кольорів певним матеріалам, таким як окуляри, на додаток до певних властивостей, притаманних атомам золота..
Синтез ауратов і руйнівного золота
Якщо додано Au2O3 до середовища, де він розчинний, і в присутності металів, аурати можуть осідати після додавання сильної основи; які, утворені аніонами AuO4- в компанії металевих катіонів.
Крім того, Au2O3 реагує з аміаком з утворенням золотого бурового з'єднання, Au2O3(NH3)4. Його назва походить від того, що він є вибухонебезпечним.
Обробка самоскладених моношарів
На золото і його оксид деякі сполуки, такі як диалкілдисульфіди, RSSR, не адсорбуються однаково. Коли відбувається ця адсорбція, спонтанно утворюється зв'язок Au-S, де атом сірки виявляє і визначає хімічні характеристики зазначеної поверхні в залежності від функціональної групи, до якої вона пов'язана..
RSSR не може адсорбуватися на Au2O3, але на металевому золоті. Тому, якщо поверхня золота і його ступінь окислення модифікуються, а також розмір частинок або шарів Au2O3, може бути розроблена більш гетерогенна поверхня.
Це поверхня Au2O3-AuSR взаємодіє з металевими оксидами певних електронних пристроїв, таким чином розвиваючи майбутніші розумніші поверхні.
Список літератури
- Вікіпедія. (2018). Оксид золота (III). Отримано з: en.wikipedia.org
- Хімічна композиція (2018). Золотий оксид (III). Відновлено з: formulacionquimica.com
- Д. Мішо. (24 жовтня 2016 року). Золоті оксиди. 911 Металург. Отримано з: 911metallurgist.com
- Ши, Р. Асахи і С. Штампфл. (2007). Властивості оксидів золота Au2O3 і Au2O: Дослідження перших принципів. Американське фізичне товариство.
- Кук, Кевін М. (2013). Золотий оксид як маскуючий шар для регіоселективної хімії поверхні. Дисертації та дисертації. Папір 1460.


