Продуктивність біологічного каталізатора і приклади
A біологічний каталізатор o біокаталізатор це молекула, в основному білкового походження, яка має здатність прискорювати хімічні реакції, що відбуваються всередині живих істот. Молекули білка каталізатора є ферментами, а молекули РНК - рибозимами. У цій статті ми зупинимося на вивченні ферментів, які є найбільш відомими біологічними каталізаторами.
За відсутності ферментів величезна кількість реакцій, що відбуваються в клітці і що дозволяють життя, не могла відбутися. Вони відповідають за прискорення процесу в порядках порядку, близьких до 106 - і в деяких випадках набагато більше.
Індекс
- 1 Каталіз
- 2 Ферменти
- 2.1 Що таке фермент?
- 2.2 Характеристики ферментів
- 2.3 Номенклатура та класифікація ферментів
- 2.4 Як працюють ферменти?
- 2.5 Ферментативні інгібітори
- 2.6 Приклади
- 3 Різниця між біологічними каталізаторами (ферментами) і хімічними каталізаторами
- 3.1 Реакції, що каталізуються ферментами, відбуваються швидше
- 3.2 Більшість ферментів працюють у фізіологічних умовах
- 3.3 Специфіка
- 3.4 Ензиматичне регулювання є точним
- 4 Посилання
Каталіз
Каталізатор являє собою молекулу, здатну змінювати швидкість хімічної реакції без споживання у зазначеній реакції.
Хімічні реакції включають енергію: початкові молекули, що беруть участь у реакції, або реагенти починаються з певної енергії. Додаткова кількість енергії поглинається для досягнення "перехідного стану". Згодом енергія вивільняється з продуктами.
Різниця енергії між реагентами і продуктами виражається як ΔG. Якщо енергетичні рівні продуктів більше, ніж реагентів, то реакція є ендергонічною і не спонтанною. Навпаки, якщо енергія продуктів нижче, реакція є ексергонічною і спонтанною.
Однак, якщо реакція є спонтанною, це не означає, що вона буде відбуватися з помітною швидкістю. Швидкість реакції залежить від ΔG * (зірочка відноситься до енергії активації).
Читач повинен пам'ятати про ці поняття, щоб зрозуміти, як відбувається функціонування ферментів.
Ферменти
Що таке фермент?
Ферменти є біологічними молекулами неймовірної складності, що складаються в основному з білків. Білки, у свою чергу, є довгими ланцюгами амінокислот.
Однією з найбільш видатних характеристик ферментів є їх специфічність у молекулі-мішені - ця молекула називається субстратом..
Характеристики ферментів
Ферменти існують у декількох формах. Деякі з них повністю складаються з білків, інші мають небілкові області, які називаються кофакторами (метали, іони, органічні молекули тощо)..
Таким чином, апофермент є ферментом без кофактора, а комбінація апоензиму і його кофактора називається голоферментом..
Це молекули значно більшого розміру. Однак тільки невелика ділянка ферменту безпосередньо бере участь у реакції з субстратом, і ця область є активним центром.
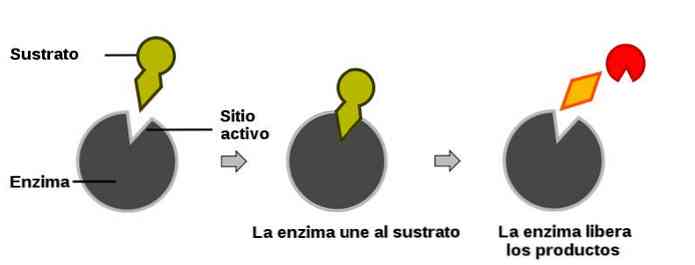
Коли починається реакція, фермент з'єднується з його субстратом, оскільки ключ пов'язаний з його замком (ця модель є спрощенням фактичного біологічного процесу, але служить для ілюстрації процесу)..
Всі хімічні реакції, які відбуваються в нашому тілі, каталізуються ферментами. Фактично, якщо б цих молекул не існувало, нам доведеться чекати сотні або тисячі років для завершення реакцій. Тому регулювання ферментативної активності необхідно контролювати дуже специфічним чином.
Номенклатура та класифікація ферментів
Коли ми бачимо молекулу, чиє ім'я закінчується в -азе, ми можемо бути впевнені, що вона є ферментом (хоча є і винятки з цього правила, як трипсин). Це конвенція для позначення назви ферментів.
Існує шість основних типів ферментів: оксидоредуктази, трансферази, гідролази, ліази, ізомерази та лігази; відповідальний за: окисно-відновну реакцію, перенесення атомів, гідроліз, додавання подвійних зв'язків, ізомеризацію і зв'язування молекул, відповідно.
Як працюють ферменти?
У розділі про каталіз ми відзначили, що швидкість реакції залежить від величини ΔG *. Чим вище це значення, тим повільніше і повільніше реакція. Фермент відповідає за зменшення зазначеного параметра - таким чином, збільшуючи швидкість реакції.
Різниця між продуктами і реагентами залишається ідентичною (фермент не впливає на нього), як і розподіл одного і того ж. Фермент сприяє формуванню перехідного стану.
Інгібітори ферментів
В контексті дослідження ферментів, інгібіторами є речовини, які здатні знижувати активність каталізатора. Вони поділяються на два типи: конкурентні та неконкурентні інгібітори. Ті першого типу конкурують з субстратом, а інші - не.
Як правило, процес інгібування є оборотним, хоча деякі інгібітори можуть залишатися пов'язаними з ферментом майже постійно.
Приклади
У наших клітинах є велика кількість ферментів - і в клітинах всіх живих істот. Однак найбільш відомими є ті, які беруть участь у метаболічних шляхах, таких як гліколіз, цикл Кребса, ланцюг транспортування електронів, серед інших..
Сукцинатдегідрогеназа являє собою фермент типу оксидоредуктази, який каталізує окислення сукцинату. У цьому випадку реакція передбачає втрату двох атомів водню.
Різниця між біологічними каталізаторами (ферментами) і хімічними каталізаторами
Існують каталізатори хімічної природи, які, подібно біологічним, збільшують швидкість реакцій. Однак існують помітні відмінності між обома типами молекул.
Реакції, що каталізуються ферментом, відбуваються швидше
По-перше, ферменти встигають збільшити швидкість реакцій в порядках близько до 106 до 1012. Хімічні каталізатори також збільшують швидкість, але лише на кілька порядків.
Більшість ферментів працюють у фізіологічних умовах
Оскільки біологічні реакції здійснюються всередині живих істот, їх оптимальні умови оточують фізіологічні значення температури і рН. Хіміки, з іншого боку, потребують різких умов температури, тиску і кислотності.
Специфіка
Ферменти дуже специфічні в реакціях, які вони каталізують. У більшості випадків вони працюють тільки з однією підкладкою або з декількома. Специфіка також стосується виду продукції, яку вони виробляють. Асортимент субстратів хімічних каталізаторів значно ширший.
Сили, що визначають специфічність взаємодії між ферментом і його субстратом, є такими ж, що диктують конформацію одного і того ж білка (взаємодії Ван-дер-Ваальса, електростатичні, водневі зв'язки і гідрофобні).
Ферментативне регулювання є точним
Нарешті, ферменти мають більшу здатність до регуляції, і активність цих ферментів залежить від концентрації різних речовин у клітині.
Серед регуляторних механізмів ми знаходимо аллостеричний контроль, ковалентну модифікацію ферментів і зміну кількості синтезованого ферменту..
Список літератури
- Berg, J. М., Stryer, L., & Tymoczko, J. L. (2007). Біохімія. Я повернувся назад.
- Кемпбелл, М. К., і Фаррелл, С. О. (2011). Біохімія Шосте видання. Томсон. Брукс / Коул.
- Девлін, Т. М. (2011). Підручник з біохімії. John Wiley & Sons.
- Koolman, J., & Röhm, K.H. (2005). Біохімія: текст і атлас. Ed. Panamericana Medical.
- Mougios, V. (2006). Вправа біохімії. Кінетика людини.
- Müller-Esterl, W. (2008). Біохімія Основи медицини та наук про життя. Я повернувся назад.
- Poortmans, J.R. (2004). Принципи фізичної вправи біохімії. Karger.
- Voet, D., & Voet, J.G. (2006). Біохімія. Ed. Panamericana Medical.


