Структура, властивості, синтез, використання та ризики натрію бензоату
The бензоат натрію є органічною сіллю, хімічною формулою якої є C6H5COONa. Він продукується або генерується реакцією нейтралізації між бензойною кислотою і гідроксидом натрію. В результаті утворюється біла тверда речовина (нижнє зображення), розчинне у воді і розкладається при нагріванні при 120 ° С.
Цю сіль можна знайти у різних фруктах та інших частинах овочів, таких як: чорниця, слива, родзинки, кориця, гвоздика та яблука. Він також є метаболітом водоростей і рослин.

Бензоат натрію не накопичується в організмі, оскільки він швидко поєднується з амінокислотою гліцин, утворюючи гіппурову кислоту, яка вільно виділяється з сечею..
Ця сполука використовується з консервантом для харчових продуктів, при цьому її дія є більш ефективною при кислому рН. Це обумовлено присутністю органічних кислот, які дають їжі рН, придатний для дії бензоату натрію; який, як такий, закінчується протонированием до бензойної кислоти.
Ця сіль також застосовується при лікуванні спадкових метаболічних порушень циклу сечовини, що виробляє накопичення проміжного метаболіту, для якого фермент, який обробляє його, є дефіцитним..
Міжнародна програма з хімічної безпеки не виявила шкідливого впливу бензоату натрію на людину при споживанні від 647 до 825 мг / кг маси тіла..
Проте повідомлялося, що бензоат натрію може викликати псевдоалергічні реакції і посилювати симптоми у пацієнтів з частими епізодами кропив'янки і астми..
Індекс
- 1 Склад бензоату натрію
- 2 Властивості
- 2.1 Хімічні назви
- 2.2 Фізичний опис
- 2.3 Запах
- 2.4 Смак
- 2.5 Точка спалаху
- 2.6 Автоматичне запалювання
- 2.7 Щільність
- 2.8 Розчинність
- 2.9 Стабільність
- 2.10 Розкладання
- 2,11 рН
- 2.12 Поверхневий натяг
- 3 Підсумок
- 4 Використання
- 4.1
- 4.2 Лікування
- 4.3 Інше
- 5 Ризики
- 6 Посилання
Склад бензоату натрію
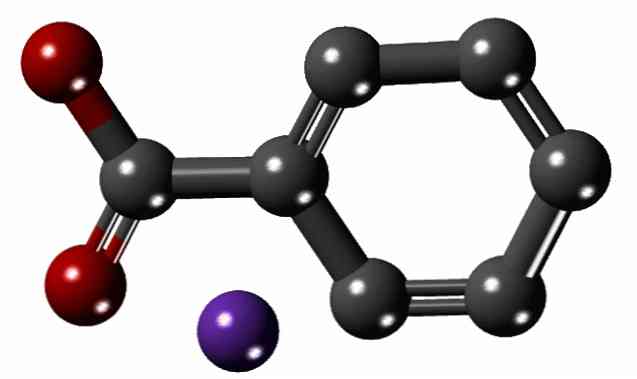
У верхньому зображенні структура бензоату натрію показана з моделлю сфер і брусів. Ароматичне кільце можна бачити неозброєним оком, з карбоксилатной групою, -COO-, пов'язані з нею (червоні сфери); і останній, у свою чергу, електростатично притягує Na катіон+ (фіолетова сфера).
Оскільки різниця в розмірах між двома іонами велика (порівняйте на зображенні), не дивно, що ретикулярна енергія кристалів бензоату натрію низька. Це призводить до того, що їхні кристали мають природну схильність до солюбілізації в полярних розчинниках або для проведення ряду хімічних реакцій.
С6H5COO- Він може приймати два водних мости від двох молекул води, що сприяє його гідратації. Тим часом Na+ Вона також закінчується сольватированной водою, долаючи електростатичні сили, які утримують її разом з С6H5COO-.
Таким чином, ця сіль складається з іонів С6H5COO- і Na+, які організовані для побудови кристалів. У літературі не наводиться жодної інформації про її кристалічну структуру, тому невідомо, який тип елементарної комірки для цієї солі.
Властивості
Хімічні назви
-Бензоат натрію
-Натрієва сіль бензойної кислоти
-Собенато
-Антимол.
Фізичний опис
Білі гранули або кристалічний порошок. Безбарвний кристалічний порошок.
Запах
Туалет.
Смак
Bittersweet, терпкий і неприємний.
Точка запалювання
> 100 ºC.
Автоматичне запалювання
> 500 ºC.
Щільність
1,50 г / см3.
Розчинність
-Розчинний в рідкому амонію і піридині.
-Трохи розчинний у етанолі: 8,22 г / 100 г при 25 ºC.
-У метанолі він більш розчинний, ніж у етанолі: 8,22 г / 100 г при 15 ºC.
Стабільність
Він є стабільним у рекомендованих умовах зберігання. Він може бути чутливим до вологи, гідролізується до бензойної кислоти. Несумісний з сильними окислювачами, лугами і мінеральними кислотами.
Розкладання
При нагріванні до розпаду при температурі 120 ° C (248 ° F) він випромінює оксид натрію та інші компоненти, які можуть бути токсичними і канцерогенними..
При розкладанні при 120 ºC це запобігає тому, що його точки кипіння і плавлення можуть бути визначені з точністю, повідомлені значення цих параметрів є теоретичними оцінками.
рН
Близько 8, розчинених у воді. Тобто це основна сіль. Це пояснюється тим, що він гідролізує для вивільнення іонів OH-.
Поверхневий натяг
72,9 мН / см при 20 ºC в розчині 1 г / л води.
Синтез
Бензойна кислота, що бере участь у синтезі бензоату натрію, виробляється в основному трьома методами:
-Нафталін окислюється пентоксидом ванадію з утворенням фталевого ангідриду. Ця сполука може зазнавати декарбоксилювання, щоб викликати бензойну кислоту, оскільки у її структурі з двома ароматичними кільцями, як видається, мають дві групи -СОО, конденсовані разом.
-Толуол окислюється до бензойної кислоти додаванням азотної кислоти. У цій реакції метильна група "просто" окислюється до карбоксильної групи:
C6H5CH3 => C6H5COOH
-І, нарешті, бензотрихлорид гідролізується дією мінеральних кислот, що походять з бензойної кислоти.
Отриману бензойну кислоту будь-яким з цих трьох способів її потім розчиняють в гідроксиді натрію. Ці сполуки піддаються реакції нейтралізації, продукуючи бензоат натрію і воду.
C6H5СООН + NaOH => C6H5COONa + H2O
Реакцію також можна проводити з карбонатом натрію, хоча його вихід може бути менше бажаного.
Використання
У їжу
Бензоат натрію є консервуючим засобом для харчових продуктів, здатним інгібувати або затримувати процес ферментації, підкислення або будь-який процес, що призводить до їх погіршення. Крім того, бензоат натрію має фунгіцидну дію.
Ця сіль здатна усунути дріжджі, бактерії і гриби, присутні в їжі. Її консервуюча дія більш ефективна при рН < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Бензоат натрію також використовується в консервації газованих напоїв і безалкогольних напоїв, в яких присутня вугільна кислота. Також в джемах, багатих лимонною кислотою, і взагалі, в харчових продуктах з присутніми кислотами, які створюють кислому середовищі.
Крім того, його використовують у кормі з концентрацією бензоату натрію 0,1%. Максимальна кількість використовуваної бензойної кислоти та бензоату натрію, як консервантів у їжі, не перевищує 2000 мг / кг їжі.
Лікування
Гостра гіперманемія
Фенилацетат натрію і бензоат натрію використовують у вигляді ад'ювантної терапії для лікування гострої гіпераммонемії та супутньої енцефалопатії у пацієнтів із змінами циклу сечовини..
Ці сполуки класифікуються як ліки-сироти. Ця деномінація стосується ліків, які з економічної точки зору не вигідно.
Шизофренія
Бензоат натрію був використаний експериментально в лікуванні шизофренії. Центральною частиною дослідження є роль, яку в лікуванні виконує інгібування ферментів оксидаз D-амінокислот, що відповідає бензоату натрію.
Аргіносукцинова кислота
Бензоат натрію застосовують при лікуванні аргініносукцинової кислоти, спадкового порушення обміну речовин, що може викликати у пацієнтів збільшення концентрації амонію, здатного впливати на центральну нервову систему..
Інгібітор
-Це інгібітор ферменту аракідонато 15-ліпоксигенази, фермент, який досліджується фармацевтичною промисловістю для участі в ішемічній хворобі серця.
-Він пригнічує дію ферменту ліпази триацилгліцеридів, ферменту, який діє на виділення гліцерину і жирних кислот в тонкому кишечнику, що дозволяє поглинати ці ліпіди, присутні в їжі.
Можливо, можна використовувати бензоат натрію для регулювання всмоктування кишечника ліпідів, таких як триацилгліцериди.
Спадкові порушення
Бензоат натрію використовується при лікуванні декількох спадкових порушень, пов'язаних з метаболізмом амінокислот, серед яких згадані: лікування гіперергінінемії та лікування дефіциту ферменту транслокази орнітину.
Інші
-Використовується в полосках на спиртовій основі і в поліруванні срібла. Крім того, він використовується при розробці піротехнічних сполук, відповідальних за свисток, що виробляється при їх загорянні.
-Використовується як антикорозійний, що є одним з основних вимог у виробництві цієї солі. Він також використовується в охолоджуючих рідинах, антифризах та інших системах на водній основі.
-При виробництві пластмас, таких як поліпропілен, він використовується для поліпшення його міцності і ясності.
-Служить стабілізатором у ванних кімнатах і фотографічних процесах.
Ризики
Бензоат натрію класифікується FDA як "загалом безпечний", в дозі 0,1% ваги їжі. Він не вважається дратівливим для шкіри та контакту з очима, тому можна сказати, що гостра токсичність низька.
Проте бензоат натрію може викликати неімунологічні реакції (псевдоалергія) при контакті. Цей ефект рідкий у нормальних людей, але у пацієнтів з частими епізодами кропив'янки або симптомів астми може спостерігатися збільшення частоти цих симптомів..
У дослідженнях на щурах і мишах не було виявлено жодних ознак канцерогенної дії бензоату натрію.
Вказувалося на незручність його використання в присутності аскорбінової кислоти, яка могла б продукувати бензол; токсичне з'єднання, позначене як канцерогенне.
Список літератури
- Чисті галузі. (2019). Виробництво бензоату натрію. Отримано з: science.jrank.org
- Вікіпедія. (2019). Бензоат натрію. Отримано з: en.wikipedia.org
- PubChem. (2019). Бензоат натрію. Отримано з: pubchem.ncbi.nim.nih.gov
- Hanes Т. (2019). Факти про бензоат натрію. Livestrong. Отримано з: livestrong.com
- Хімічна книга. (2017). Бензоат натрію. Отримано з: chemicalbook.com
- Lane H. et al. (2013) Jama Psichiatry. 70 (12): 1267-1275.
- Всесвітня організація охорони здоров'я Женева. (12 квітня 2005 р.) Бензойна кислота і бензоат натрію. [PDF] Отримано з: who.int


