Властивості етилового ефіру, структура, отримання, застосування
The етиловий ефір, також відомий як діетиловий ефір, являє собою органічну сполуку, хімічна формула якої є C4H10О. Він характеризується тим, що він є безбарвною і летючою рідиною, і тому його пляшки повинні бути максимально герметично закриті..
Цей ефір класифікують як член диалкилових ефірів; тобто вони мають формулу ROR ', де R і R' являють собою різні вуглецеві сегменти. І як він описує своє середнє ім'я, діетиловий ефір, це два радикали-етил ті, що зв'язуються з атомом кисню.

Спочатку етиловий ефір використовувався як загальний анестетик, введений в 1846 році Вільямом Томасом Зеленим Мортоном. Однак, через його горючість, його використання було відкинуто, замінивши його іншими менш небезпечними анестетиками..
Ця сполука також використовувалася для оцінки часу кровообігу, при оцінці стану серцево-судинного стану пацієнтів.
В організмі діетиловий ефір може бути перетворений у вуглекислий газ і метаболіти; остання закінчується виділенням з сечею. Однак більша частина введеного ефіру видихається в легенях, не зазнаючи жодної модифікації.
З іншого боку, він використовується як розчинник для мила, масел, парфумерії, алкалоїдів і ясен.
Індекс
- 1 Структура етилового ефіру
- 1.1 Міжмолекулярні сили
- 2 Фізико-хімічні властивості
- 2.1 Інші назви
- 2.2 Молекулярна формула
- 2.3 Молекулярна маса
- 2.4 Фізичний вигляд
- 2.5 Запах
- 2.6 Смак
- 2.7 Точка кипіння
- 2.8 Температура плавлення
- 2.9 Точка спалаху
- 2.10 Розчинність у воді
- 2.11 Розчинність в інших рідинах
- 2.12 Щільність
- 2.13 Щільність пари
- 2.14 Тиск пари
- 2.15 Стабільність
- 2.16 Автоматичне запалювання
- 2.17 Декомпозиція
- 2.18 В'язкість
- 2.19 Теплота згоряння
- 2.20 Теплота випаровування
- 2.21 Поверхневий натяг
- 2.22 Іонізаційний потенціал
- 2.23 Поріг запаху
- 2.24 Показник заломлення
- 3 Отримання
- 3.1 З етилового спирту
- 3.2 З етилену
- 4 Токсичність
- 5 Використання
- 5.1 Органічний розчинник
- 5.2 Загальна анестезія
- 5.3. Дух ефіру
- 5.4 Оцінка кровообігу
- 5.5 Навчальні лабораторії
- 6 Посилання
Структура етилового ефіру
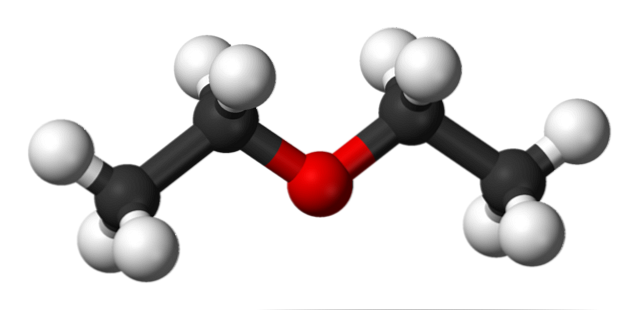
На зображенні вище ми маємо уявлення з моделлю сфер і смуг молекулярної структури етилового ефіру.
Як видно, червона сфера, що відповідає атому кисню, має дві етільні групи, пов'язані з обох сторін. Всі ланки прості, гнучкі і вільно обертаються навколо осей σ.
Ці повороти походять зі стереоізомерів, відомих як конформери; що більше, ніж ізомери, вони є альтернативними просторовими станами. Структура зображення відповідає саме антиконформі, в якому всі її групи атомів розташовані в шаховому порядку (відокремлені один від одного).
Яким буде інший конформер? Затьмарені, і хоча ваше зображення недоступне, просто візуалізуйте його у формі U. На верхніх кінцях U будуть розташовані метильні групи, -CH.3, які мали б стеричні відштовхування (вони стикалися б у просторі).
Тому очікується, що молекула СН3CH2OCH2CH3 прийняти антиконформацію більшу частину часу.
Міжмолекулярні сили
Якими міжмолекулярними силами є молекули етилового ефіру, що регулюються в рідкій фазі? Вони зберігаються в рідині переважно завдяки дисперсійним силам, оскільки в їх дипольному моменті (1.5D) відсутня область, достатньо дефіцитна по електронній щільності (δ +).
Це пояснюється тим, що жоден атом вуглецю етильних груп не дає занадто великої електронної щільності для атома кисню. Вищезгадане видно з карти електростатичного потенціалу етилового ефіру під рукою (нижнє зображення). Зверніть увагу на відсутність синьої області.
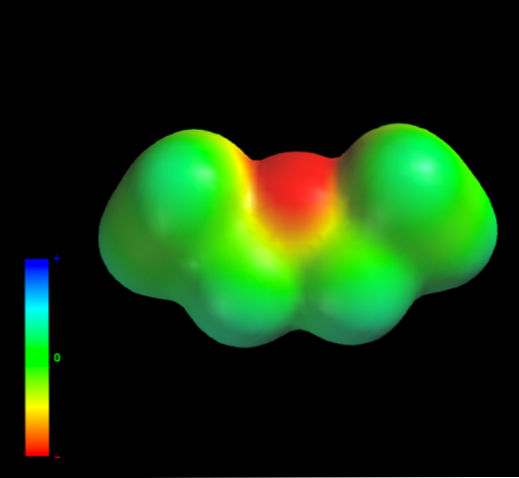
Кисень теж не може утворювати водневі зв'язки, тому що в молекулярній структурі відсутні O-H зв'язки. Тому миттєві диполи і їх молекулярна маса сприяють їх розсіюванню.
Незважаючи на це, він добре розчинний у воді. Чому? Оскільки його атом кисню з більш високою електронною щільністю, може приймати водневі зв'язки з молекули води:
(CH3CH2)2Oδ- - δ+H-OH
Ці взаємодії обумовлюють розчинення 6,04 г цього ефіру в 100 мл води.
Фізико-хімічні властивості
Інші назви
-Діетиловий ефір
-Етоксиэтан
-Етилоксид
Молекулярна формула
C4H10O або (C2H5)2O.
Молекулярна маса
74,14 г / моль.
Зовнішній вигляд
Безбарвна рідина.
Запах
Солодкий і пряний.
Смак
Палаючий і солодкий.
Точка кипіння
94,3 ºF (34,6 ºC) до 760 мм рт.
Точка плавлення
-177,3 ° F (-116,3 ° C). Стабільні кристали.
Точка запалювання
-49ºF (закритий контейнер).
Розчинність у воді
6,04 г / 100 мл при 25 ° С.
Розчинність в інших рідинах
Змішується з коротколанцюговими аліфатичними спиртами, бензолом, хлороформом, петролейним ефіром, жировим розчинником, багатьма маслами і концентрованою соляною кислотою.
Розчинний в ацетоні і дуже розчинний у етанолі. Він також розчинний у нафті, бензолі і маслах.
Щільність
0,714 мг / мл при 68 ° F (20 ° C).
Щільність пари
2.55 (по відношенню до повітря, взятого з щільністю 1).
Тиск пари
442 мм рт.ст. при 68ºF. 538 мм рт.ст. при 25 ° С. 58,6 кПа при 20 ºC.
Стабільність
Він повільно окислюється дією повітря, вологи і світла з утворенням пероксидів.
Утворення пероксидів може відбуватися в ефірних контейнерах, які були відкриті і які зберігаються на зберіганні більше шести місяців. Пероксиди можуть детонуватися шляхом тертя, удару або нагрівання.
Уникати контакту з: цинком, галогенами, неметалевими оксигалогенідами, сильними окислювачами, хромилхлоридом, тементиновими маслами, нітратами та хлоридами металів.
Автоматичне запалювання
356ºF (180ºC).
Розкладання
При розігріві він розкладається, виділяючи різкий і дратівливий дим.
В'язкість
0,2448 cPoise при 20 ºC.
Теплота згоряння
8,807 ккал / г.
Випаровування тепла
89,8 кал / г при 30 ° С.
Поверхневий натяг
17.06 дин / см при 20º C.
Іонізаційний потенціал
9,53 еВ.
Поріг запаху
0,83 ppm (чистота не вказана).
Індекс заломлення
1,355 при 15 ºC.
Отримання
З етилового спирту
Етиловий ефір може бути отриманий з етилового спирту, в присутності сірчаної кислоти в якості каталізатора. Сірчана кислота у водному середовищі дисоціює, продукуючи іон гідронію, Н3O+.
Безводний етиловий спирт протікає через розчин сірчаної кислоти, нагрітий між 130 ° C і 140 ° C, виробляючи протонирование молекул етилового спирту. Згодом інша молекула непротонованого етилового спирту вступає в реакцію з протонированной молекулою.
Коли це відбувається, нуклеофільна атака другої молекули етилового спирту сприяє вивільненню води з першої молекули (протонированной); в результаті утворюється протонированний етиловий ефір (СН3CH2OHCH2CH3), з частково зарядженим киснем позитивним.
Однак цей спосіб синтезу втрачає ефективність, оскільки сірчана кислота розбавляється водою, що утворюється в процесі (продуктом зневоднення етилового спирту)..
Температура реакції є критичною. При температурі нижче 130 ° C реакція відбувається повільно і здебільшого етиловий спирт переганяється.
Вище 150 ° С сірчана кислота викликає утворення етилену (подвійний зв'язок алкена) замість об'єднання з етиловим спиртом з утворенням етилового ефіру..
З етилену
У протилежному процесі, тобто гідратації етилену в паровій фазі, етиловий ефір може бути сформований як побічний продукт на додаток до етилового спирту. Фактично, цей синтетичний шлях виробляє більшу частину цієї органічної сполуки.
У цьому процесі використовують каталізатори фосфорної кислоти, прикріплені до твердої основи, здатні регулюватися для отримання більшого кількості ефіру.
Дегідратація в паровій фазі етанолу в присутності алюмооксидних каталізаторів може давати 95% вихід у виробництві етилового ефіру..
Токсичність
Це може викликати подразнення на шкірі і очах при контакті. Контакт з шкірою може викликати його висихання і розтріскування. Ефір зазвичай не проникає в шкіру, оскільки він швидко випаровується.
Роздратування очей, спричинене ефіром, зазвичай м'яке, а у випадку сильного роздратування, пошкодження зазвичай оборотно.
Її прийом викликає наркотичні ефекти і роздратування шлунка. Тяжке проковтування може викликати пошкодження нирок.
Вдихання ефіру може викликати подразнення носа і горла. У разі інгаляції може виникнути ефір: сонливість, збудження, запаморочення, блювота, нерівномірне дихання і підвищене слиновиділення.
Висока експозиція може призвести до втрати свідомості і навіть смерті.
OSHA встановлює межу професійної експозиції в середньому 800 ppm протягом 8-годинної зміни.
Рівні подразнення очей: 100 ppm (людські). Рівні подразнення очей: 1200 мг / м3 (400 ppm).
Використання
Органічний розчинник
Це органічний розчинник, який використовується для розчинення брому, йоду та інших галогенів; більшість ліпідів (жирів), смол, чистих каучуків, деяких алкалоїдів, ясен, парфумерії, ацетату целюлози, нітрату целюлози, вуглеводнів і барвників.
Крім того, він використовується при витяганні активних речовин тканин і рослин тварин, оскільки має більш низьку щільність, ніж вода і плаває на ній, залишаючи бажані речовини розчиненими в ефірі..
Загальна анестезія
Вона використовується як загальний анестетик з 1840 року, замінюючи хлороформ на терапевтичну перевагу. Проте воно є легкозаймистим речовиною, і тому стикається з важкими труднощами для його використання в клінічних умовах.
Крім того, він виробляє у пацієнтів деякі небажані післяопераційні побічні ефекти, такі як нудота і блювота.
З цих причин використання ефіру як загальної анестезії було відкинуто, замінивши його іншими анестетиками, такими як галотан..
Дух ефіру
Ефір, змішаний з етанолом, використовували для утворення розчину, що називається спиртом ефіру, використовуваним при лікуванні метеоризму шлунка і більш легких форм гастралгії..
Оцінка кровообігу
Ефір використовується для оцінки кровообігу між рукою і легенями. Ефір вводять в руку, приводячи кров до правого передсердя, потім до правого шлуночка і звідти в легені.
Час, що проходить від ін'єкції ефіру, до поглинання ефірного запаху у видихуваному повітрі становить приблизно від 4 до 6 с..
Навчальні лабораторії
Ефір використовують у навчальних лабораторіях у багатьох експериментах; наприклад, в демонстрації законів Менделя про генетику.
Ефір використовується для оніміння мух роду Drosophila і забезпечення необхідних перетинів між ними, для того, щоб засвідчити закони генетики
Список літератури
- Грем Соломонс Т.В., Крейг Б. Фріле. (2011). Органічна хімія. Аміни (10й видання.). Wiley Plus.
- Кері Ф. (2008). Органічна хімія (Шосте видання). Mc Graw Hill.
- Sevier. (2018). Діетиловий ефір. Наука Пряма. Отримано з: sciencedirect.com
- Редактори Британської енциклопедії. (2018). Етиловий ефір. Britannica ncyclopædia. Отримано з: britannica.com
- PubChem (2018). Ефір. Отримано з: pubchem.ncbi.nlm.nih.gov
- Вікіпедія. (2018). Діетиловий ефір. Отримано з: en.wikipedia.org
- Лист безпеки XI: етиловий ефір. [PDF] Відновлено з: quimica.unam.mx


